中国海洋湖沼学会主办。
文章信息
- 李进京, 刘颖, 李祥付, 刘好真, 徐鹏, 孙元, 焦海峰, 王一农, 尤仲杰. 2020.
- LI Jin-Jing, LIU Ying, LI Xiang-Fu, LIU Hao-Zhen, XU Peng, SUN Yuan, JIAO Hai-Feng, WANG Yi-Nong, YOU Zhong-Jie. 2020.
- 韭山列岛海洋生态自然保护区及其附近海域底拖网生物资源的分布及群落结构分析
- DISTRIBUTION AND COMMUNITY STRUCTURE OF TRAWLING MARINE ORGANISMS IN JIUSHAN ISLANDS MARINE ECOLOGICAL NATURE RESERVE AND ADJACENCY
- 海洋与湖沼, 51(1): 176-185
- Oceanologia et Limnologia Sinica, 51(1): 176-185.
- http://dx.doi.org/10.11693/hyhz20191000195
文章历史
-
收稿日期:2019-10-22
收修改稿日期:2019-11-20
2. 中国科学院南海海洋研究所 广州 510301;
3. 浙江省宁波市海洋与渔业研究院 宁波 315103
2. Oceanography South China Sea Institute of Oceanology Chinese Academy of Sciences, Guangzhou 510301, China;
3. Zhejiang Ningbo Academy of Oceanology and Fishery, Ningbo 315103, China
海洋生物调查可用于研究海域生物的物种组成、时空分布及群落结构, 对于比较和分析海域生态特征有重要意义(Rizkalla et al, 2016; Sovkan et al, 2016; Stevenson et al, 2019), 海洋生物调查已广泛应用于我国海域(张洪亮等, 2012; 张亮等, 2014; 于鑫等, 2017; 张敬怀等, 2017), 对于自然生态保护区及其附近海域的对比研究, 能反映人为活动对海域的影响, 并一定程度反映保护区的保护成效(田甲申等, 2013)。
韭山列岛位于浙江省东部海域, 生物资源丰富, 生态环境优良, 2011年被列为国家级海洋生态自然保护区, 保护区内严禁任何生产性经营活动, 自然生态系统受到严格保护(卢衎尔等, 2019)。海洋生物资源调查已应用于韭山列岛附近海域(张洪亮等, 2008), 主要研究了韭山列岛水生生物及主要鱼类的资源量(张亚洲等, 2013)、虾类生态位宽度和生态位重叠值及其与环境因子的关系(徐开达等, 2018; 卢衎尔等, 2019), 并研究了韭山列岛的潮间带底栖生物多样性(贺舟挺等, 2012), 而对于韭山列岛自然保护区的保护效果, 及其与附近海域的比较分析未见报道。
本研究通过2个航次的海域底拖网生物调查, 运用物种多样性指数、丰度生物量比较曲线(abundance- biomass comparison curves, ABC)、相似性聚类(Bray-Curtis)及非度量多维尺度分析(non-metric multi-dimensional scali ng, NMDS)等方法, 比较分析了春、夏季韭山列岛海洋生态自然保护区及其附近海域底拖网生物资源的种类组成、特征种、季节更替率、时空分布、群落结构、受干扰程度以及环境因子的相关性, 为韭山列岛海洋生态自然保护区及其附近海域的生物种群分布、群落结构特征、受干扰情况的差异性及保护区建设成效提供评价依据和参考。
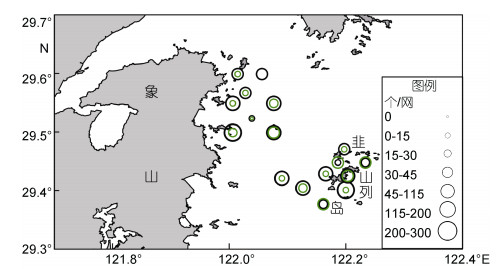
1 材料与方法 1.1 调查站位及采样时间按照《海洋调查规范》(中华人民共和国国家质量监督检验检疫总局, 2008b), 于2012年4月(春)、2012年7月(夏)在避开航道与岛礁的基础上在韭山列岛海洋生态自然保护区(下简称保护区)及其附近海域共设立17个调查站位, 进行了底拖网生物调查。其中保护区附近海域设8个站位(S01—S08), 保护区设9个站位(S09—S17), 站位分布图由Surfer 11.0绘制, 底图来自国家地理信息公共服务平台非涉密测绘地理信息(图 1)。
 |
| 图 1 韭山列岛海洋生态自然保护区及其附近海域调查站位分布 Fig. 1 Distribution of sampling station in the Jiushan Islands Marine Ecological Nature Reserve and the adjacency |
采样拖网为阿氏网(网口高1.5m, 网口宽0.5m, 网身长5m, 囊网网目为25mm), 船速为2kn/h, 各调查站位拖网时间为10min。拖网所获样本经20目筛网冲洗后用7%福尔马林现场固定, 并带回实验室进行种类鉴定、计数、称量。各站位使用抓斗式采泥器(DP-QNC6-1)采集沉积物, 带回实验室进行沉积物粒径分析(激光粒度分布仪, BT-9300ST)。根据沉积物粒度组成比例, 分为黏土(Clay)、粉砂(Silt)、砂(Sand) (Flemming, 2000)。采集各站位表层水样(距水表层0.5m)及底层水样(距底部0.5m), 运用分光光度法测定叶绿素, 并运用黑白瓶法测定表层及底层初级生产力。海上采样及样本处理工作按照《海洋调查规范》中华人民共和国国家质量监督检验检疫总局, 2008a, b)执行, 生物种类鉴定参照中国动物主题数据库。
1.3 数据计算与分析 1.3.1 丰度与生物量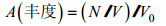
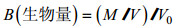
式中, A表示丰度, 单位为个/网(ind/Agt), B为生物量, 单位为克/网(g/Agt)。N、M分别为样本数量和质量, V为实际拖网过水体体积, V0为航速2节、时间10min情况下拖网的过水体积的数值, 其值为463。
1.3.2 物种季节更替率、特征种及贡献率运用物种季节更替率R计算所获物种季节更替情况, 计算公式如下:
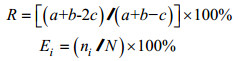
式中, a与b分别为相邻2个季节的物种数, c为相邻2个季节的共同物种数; Ei表示物种i的贡献率, ni为航次物种i的丰度。在群落总丰度中, 物种i丰度占群落总丰度的比例表示贡献率, 以贡献率大于5%的物种作为特征种(杜飞雁等, 2011, 2013)。
1.3.3 生物多样性指数采用Shannon-Weiner多样性指数(H)、Margalef物种丰富度指数(D)与Pielou均匀度指数(J)对拖网所获生物多样性进行分析(Margalef, 1958; Pielou, 1975; Ludwig et al, 1988), 公式如下:
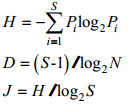
式中, Pi为第i种的个数与样品中的总个数的比值, N为样品中所有种类的总个数, S为样品中的种类总数, 数据的计算通过软件Excel 2016进行。
1.3.4 群落结构分析各站位丰度值经过2次方根转化后, 利用Past 3软件中的Bray-Curtis相似性系数及多维排序尺度方法(non-metric multi-dimensional scaling, NMDS)对群落结构进行分析。利用丰度生物量比较曲线(abundance-biomass comparison curves, ABC)来参考判断人类活动或环境污染对底拖网生物群落的扰动情况, 用w(胁强系数)作为ABC曲线的一个统计量(Warwick, 1986), 公式如下:

式中, Bi和Ai为ABC曲线中种类序号对应的生物量和数量的累积百分比, S为出现物种数。当生物量优势度曲线在数量优势度之上时, w为正, 反之为负(邓小艳等, 2018)。
1.3.5 群落分布生物及环境因子相关性分析运用Spearman相关分析法(SPSS 22.0)对海域拖网海洋生物群落分布的物种数、生物量、丰度及环境因子进行相关性分析(因砂的含量极低 < 1%, 分析时予以忽略), 包括各站位的物种数、生物量、丰度、经度、纬度、中值粒径(D50)、黏土含量、砂含量、表层水叶绿素、底层水叶绿素、表层初级生产力、底层初级生产力。
2 结果与分析 2.1 种类组成、特征种及季节更替率 2.1.1 种类组成共获得海洋生物45属47种, 隶属7门11纲22目36科。所获海洋生物节肢动物门(Arthropoda)、软体动物门(Mollusca)、脊索动物门(Chordata)累积百分比为78%, 其中节肢动物物种所占比例最多(37%)。保护区及其附近海域春季、夏季的生物类群与全海域生物类群组成相近, 保护区生物种类数高于其附近海域(表 1)。
| 类群 | 物种数 | ||||||
| 保护区 | 附近海域 | 保护区(春) | 附近海域(春) | 保护区(夏) | 附近海域(夏) | 全海域 | |
| 节肢动物门 | 16 | 16 | 10 | 6 | 15 | 15 | 17 |
| 软体动物门 | 9 | 4 | 6 | 3 | 5 | 2 | 10 |
| 脊索动物门 | 9 | 8 | 3 | 4 | 8 | 7 | 10 |
| 棘皮动物门 | 3 | 4 | 2 | 4 | 2 | 0 | 4 |
| 刺胞动物门 | 3 | 3 | 1 | 2 | 3 | 1 | 4 |
| 环节动物门 | 1 | 1 | 1 | 1 | 0 | 1 | 1 |
| 栉水母动物门 | 1 | 1 | 1 | 0 | 1 | 1 | 1 |
| 合计 | 42 | 37 | 24 | 20 | 34 | 27 | 47 |
春季保护区特征种有7种, 4种为甲壳纲生物, 底栖鱼类、刺胞动物、软体动物各1种; 保护区附近海域特征种有7种, 4种为甲壳纲生物, 底栖鱼类1种, 软体动物2种。夏季保护区特征种有5种, 4种为甲壳纲动物, 栉水母动物1种; 保护区附近海域特征种4种, 均为甲壳纲生物。日本鼓虾(Alpheus japonicas)为2季的共有特征种。春季贡献率最高物种为日本鼓虾, 贡献率为32.104%(保护区), 贡献率为20.932%(附近海域), 夏季保护区贡献率最高物种为哈氏仿对虾, 贡献率为23.948%, 保护区附近海域为葛氏长臂虾, 贡献率为28.907%(表 2)。
| 物种(特征种) | 贡献率(%) | |||
| 保护区(春) | 附近海域(春) | 保护区(夏) | 附近海域(夏) | |
| 日本鼓虾Alpheus japonicas | 32.104 | 20.932 | 5.753 | 23.401 |
| 葛氏长臂虾Palaemon gravieri | 7.778 | 7.398 | — | 28.907 |
| 哈氏仿对虾Parapenaeopsis hardwickii | — | 5.827 | 23.948 | — |
| 中华管鞭虾Solenocera crassicornis | — | — | 9.893 | 9.170 |
| 细螯虾Leptochela gracilis | — | 10.584 | — | — |
| 细巧仿对虾Parapenaeopsis tenella | 6.354 | — | — | — |
| 口虾蛄Oratosquilla oratoria | 5.500 | — | 6.389 | 6.874 |
| 红狼牙鰕虎鱼Odontamblyopus rubicundus | 5.291 | 6.669 | — | — |
| 球形侧腕水母Pleurobranchia globosa | — | — | 5.694 | — |
| 强壮仙人掌Cavernularia habereri | 6.341 | — | — | — |
| 裁判螺Brachytoma flavidulus | — | 9.836 | — | — |
| 小荚蛏Siliqua minima | 8.378 | 5.085 | — | — |
| 注“—”表示贡献率低于5% | ||||
2航次采样共有种有21种, 季节物种更替率为54.35%。保护区季节共有种为15种, 季节物种更替率为64.29%;保护区附近海域季节共有种为10种, 季节物种更替率为72.97%。保护区季节物种更替率高于其附近海域。
2.2 丰度、生物量时空分布 2.2.1 丰度的时空分布保护区各站位平均丰度为37.459ind/Agt, 保护区附近海域平均丰度为37.048ind/Agt。春季丰度高值出现在保护区站位S13、S15、S16及附近海域的站位S5、S8;夏季丰度高值出现在保护区站位S12、S13、S14、S16、S17及其附近海域站位S4、S5、S7、S8。总体上, 保护区中部和西部站位丰度较高; 保护区附近海域远离象山港入海口的站位丰度较高, 其中春季远岸侧丰度较高, 夏季近岸侧较高(图 2)。
 |
| 图 2 春季、夏季韭山列岛海洋生态自然保护区及其附近海域丰度的空间分布 Fig. 2 Spatial and seasonal distribution of abundance in sampling stations of the Jiushan Islands Marine Ecological Nature Reserve and the adjacency 注:黑色圆圈表示夏季, 绿色表示春季 |
保护区生物量均值为59.160g/Agt, 保护区附近海域均值为37.230g/Agt。春季生物量高值出现在保护区中部站位S13及保护区附近海域的站位S5、S7、S8;夏季生物量高值出现在站位S13、S14, 保护区附近海域站位S4、S7。总体上, 保护区中部和南部站位生物量较高; 保护区附近海域远离象山港入海口的站位生物量较高, 其中春季远岸侧生物量较高, 夏季近岸侧较高(图 3)。
 |
| 图 3 春季、夏季韭山列岛海洋生态自然保护区及其附近海域生物量的空间分布 Fig. 3 Spatial and seasonal distribution of biomass in sampling stations of the Jiushan Islands Marine Ecological Nature Reserve and the adjacency 注:黑色圆圈表示夏季, 绿色表示春季 |
群落分布相关因子丰度、生物量、物种数相互之间呈极显著相关性(< 0.01), 丰度与生物量和物种数相关性大于生物量和物种数间相关性。D50与黏土和粉砂呈极显著相关性, 底部初级生产力分别与表层初级生产力和纬度之间呈显著相关性(< 0.05)。D50、黏土、粉砂相关系数较大, 其中D50、粉砂接近1, 黏土与D50、粉砂之间接近-1。底部初级生产力与表层生产力呈正相关, 与纬度呈负相关(表 3)。
| 变量 | A | B | S | D50 | C | SL | PP1 | PP2 | LT |
| A | 1 | ||||||||
| B | 0.885# | 1 | |||||||
| S | 0.895# | 0.786# | 1 | ||||||
| D50 | 0.081 | –0.054 | 0.065 | 1 | |||||
| C | –0.147 | –0.061 | –0.080 | –0.828# | 1 | ||||
| SL | 0.147 | 0.061 | 0.080 | 0.828# | –1.000# | 1 | |||
| PP1 | 0.167 | 0.163 | 0.227 | –0.052 | –0.243 | 0.243 | 1 | ||
| PP2 | 0.020 | 0.051 | 0.209 | –0.047 | 0.093 | –0.093 | 0.491* | 1 | |
| LT | 0.141 | 0.118 | –0.125 | –0.359 | 0.303 | –0.303 | –0.219 | –0.571* | 1 |
| 注: “#”表示极显著相关性(显著性 < 0.01); “*”表示显著相关性(显著性 < 0.05)。A:丰度; B:生物量; S:物种数; D50:中值粒径; C:黏土; SL:粉砂; PP1:表层初级生产力; PP2:底层初级生产力; LT:纬度, 仅列出显著性因子 | |||||||||
群落分布相关因子丰度与生物量、物种数呈极显著正相关性, 与D50、粉砂、纬度呈显著正相关性与黏土、经度呈负显著相关性。生物量与丰度呈极显著正相关性, 与物种数、D50、黏土、粉砂、经度呈显著相关性。D50与黏土、粉砂呈极显著相关性, 与5m初级生产力呈显著相关性。表层叶绿素与底部叶绿素呈显著正相关性。底部初级生产力与D50、粉砂呈显著正相关性, 与黏土呈负显著相关性。夏季与春季相比, 物种数、丰度、生物量相互均有显著相关性, 夏季物种数、丰度、生物量与多种环境因子有显著相关性(表 4)。
| A | B | S | D50 | CL | SL | Chl-1 | Chl-2 | PP2 | LG | LT | |
| A | 1 | ||||||||||
| B | 0.725# | 1 | |||||||||
| S | 0.644# | 0.581* | 1 | ||||||||
| D50 | 0.531* | 0.502* | 0.231 | 1 | |||||||
| CL | –0.556* | –0.564* | –0.220 | –0.990# | 1 | ||||||
| SL | 0.556* | 0.564* | 0.220 | 0.990# | –1.000# | 1 | |||||
| Chl-1 | 0.151 | 0.126 | 0.049 | 0.252 | –0.231 | 0.231 | 1 | ||||
| Chl-2 | –0.007 | 0.181 | –0.031 | 0.119 | –0.132 | 0.132 | 0.590* | 1 | 1 | ||
| PP2 | –0.403 | –0.287 | –0.481 | –0.526* | 0.506* | –0.506* | 0.035 | 0.002 | |||
| LG | –0.562* | –0.495* | –0.334 | –0.044 | 0.077 | –0.077 | 0.118 | 0.249 | 0.053 | 1 | |
| LT | 0.564* | 0.179 | 0.472 | 0.058 | –0.066 | 0.066 | 0.274 | –0.12 | –0.300 | –0.452 | 1 |
| 注: “#”表示极显著相关性(显著性 < 0.01); “*”表示显著相关性(显著性 < 0.05)。A:丰度; B:生物量; S:物种数; D50:中值粒径; C:黏土; SL:粉砂; Chl-1:表层叶绿素; Chl-2:底层叶绿素; PP1:表层初级生产力; PP2:底层初级生产力; LG:经度; LT:纬度, 仅列出显著性因子 | |||||||||||
保护区Shannon-Weiner指数、Pielou’s evenness指数、Margalef指数春季低于夏季, 保护区附近海域Shannon-Weiner指数、Margalef指数多样性指数春季低于夏季, Pielou’s evenness指数春季较高, 夏季处于较低水平; 总体上, 多样性指数春季保护区附近海域较高, 夏季保护区较高(表 5)。
| 研究海域 | 生物多样性指数 | |||||
| H1 | J1 | D1 | H2 | J2 | D2 | |
| 保护区 | 2.083±0.681 | 0.815±0.742 | 1.504±0.510 | 0.051±0.418 | 0.842±0.038 | 2.159±0.482 |
| 保护区附近海域 | 2.359±0.474 | 0.882±0.089 | 1.541±0.311 | 2.951±0.405 | 0.821±0.133 | 2.054±0.241 |
| 注: H1、J1、D1分别表示春季Shannon-Weiner指数、Pielou’s evenness、Margalef指数H2、J2、D2分别表示夏季Shannon-Weiner指数、Pielou’s evenness、Margalef指数 | ||||||
春季H、J、D高值区分布于保护区的中东部和保护区附近海域远离象山港入海口和保护区之间区域的西部, 远离大陆海域。低值区位于保护区北部、西部和其附近海域近海岸侧。夏季H、J、D高值区分布于保护区附近海域的象山港入海口附近及远离大陆海域, 由西北向东南延伸, 至保护区的西北部, 低值区分布于保护区附近海域远离入海口临近大陆海域及保护区的西南部。夏季多样性指数高值范围高于春季, 春季保护区低值区少于其附近海域, 总体上, 多样性指数具有春、夏季相近的趋势(图 4)。
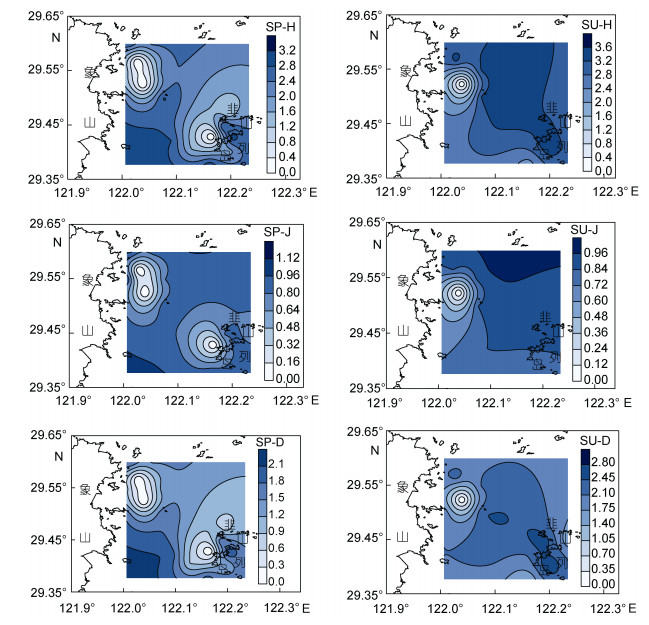 |
| 图 4 Shannon-Weiner指数、Pielou’s evenness指数、Margalef物种丰富度指数的春夏季节空间分布图 Fig. 4 The seasonal spatial contour distributions of the Shannon-Weiner index, Pielou's evenness index, Margalef index 注: SP-H、SU-H表示春、夏季多样性指数; SP-J、SU-J表示春、夏季均匀度指数; SP-D、SU-D表示春夏季丰富度指数 |
春季相似系数在10%—80%之间, 在20%—26%相似水平上物种聚集为4个群组, 对照站位图可以发现春季保护区附近海域靠近入海口一侧与远离入海口被分到不同群组(S05、S08与S02、S03), 保护区与其附近海域未被完全分开, 站位群落存在相近情况; 夏季相似系数在20%—65%之间, 在31%—35%相似水平上物种被聚集为个4群组, 保护区和其附近海域被分到不同群组(S01—S08与S09—S17), 聚类分析与NMDS分析结果一致(图 5)。
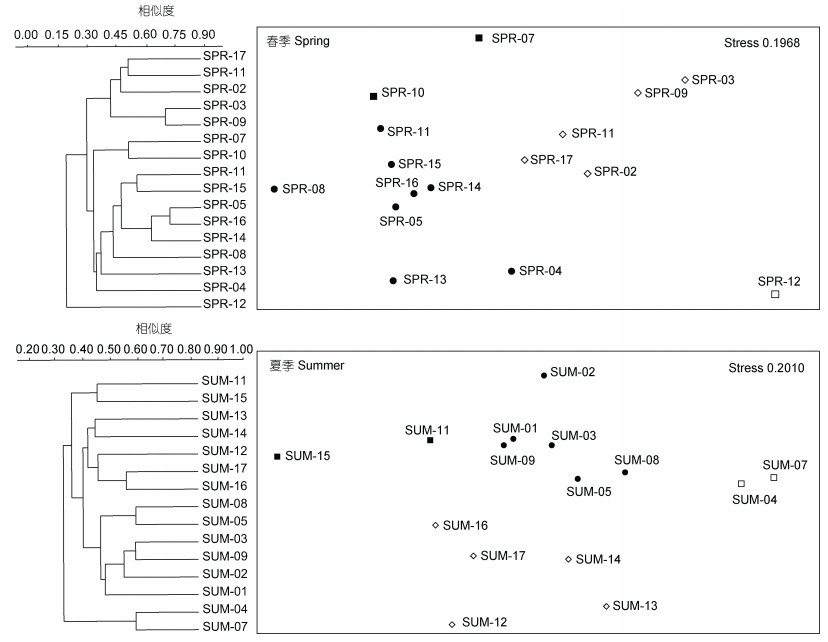 |
| 图 5 春季、夏季底拖网海洋生物聚类分析(Bray-Curtis)与非度量多维排序尺度分析(NMDS) Fig. 5 The cluster analysis (Bray-Curtis) and non-metric multi-dimensional scaling analysis (NMDS) on trawling marine organisms in spring and summer 注:圆点、菱形、实心正方形、空心正方形用以区分非度量多维排序尺度分析的不同群组 |
春季保护区生物量累积曲线基本上在丰度累积曲线之的上部, w值为正, 表明春季保护区处于轻微扰动状态, 保护区附近海域生物量累积曲线在丰度累积曲线之上, w值为正, 表明春季保护区附近海域生物群落处于稳定状态, 未受到干扰; 夏季春季保护区生物量累积曲线基本上在丰度累积曲线之的上部, w值为正, 表明夏季保护区处于轻微扰动状态, 保护区附近海域生物量累积曲线大部分在丰度累积曲线之下, w为负, 表明夏季保护区附近海域生物群落受到重度干扰(图 6)。
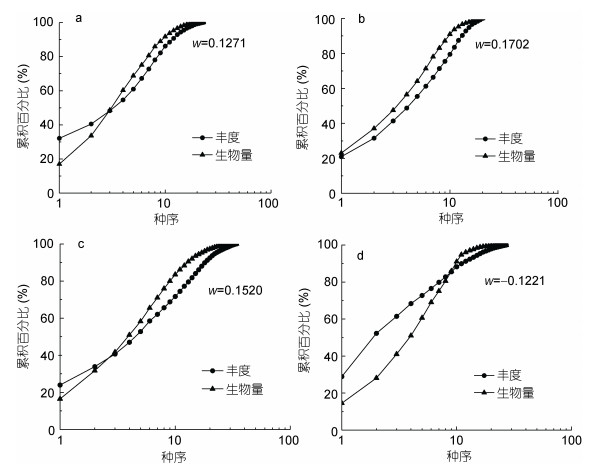 |
| 图 6 春季、夏季丰度生物量比较曲线 Fig. 6 The ABC plots in spring and summer 注: a表示春季保护区, b表示保护区附近海域, c表示夏季保护区, d表示夏季保护区附近海域 |
研究海域共获得底拖网海洋生物45属47种, 其中保护区物种总数42种(春季24种, 夏季34种)高于其附近海域37种(春季20种, 夏季27种), 物种组成的不同导致季节间物种的区域差异。春季保护区节肢动物种数(10种)与软体动物种数(6种)高于其附近海域节肢动物种数(6种)与软体动物种数(3种); 夏季保护区软体动物数(5种)高于附近海域软体动物数(2种)(表 1)。保护区和与其附近海域的生物类群组成相近, 但同时保护区和附近海域类群的具体物种数存在差异, 从而导致保护区与其附近海域物种组成存在差异, 该现象与多个海域一致(徐友伟等, 2015; Song et al, 2016; 曲慧敏等, 2017), 其原因可能是保护区和其附近海域位置相近, 其物种可以发生一定程度的迁移和交换, 使得物种类群组成相近(Mace et al, 2019); 保护区因受到保护, 人为活动对其影响较小(卢衎尔等, 2019), 物种季节更替率小于保护区附近海域, 使得物种的延续性较高, 从而使得保护区物种数高于其附近海域。
3.2 丰度、生物量的时空分布差异保护区平均丰度(37.459ind/Agt)略高于其附近海域(37.048ind/Agt), 平均生物量(59.160g/Agt)远高于其附近海域(37.230g/Agt), 保护区个体平均生物量较高, 主要是保护区内禁止各种形式的人为捕渔生产活动, 物种个体生物量增加, 与其附近海域相比, 物种体型可以生长到更大(王金宝等, 2017; 卢衎尔等, 2019)。保护区附近海域远离象山港入海口的站位丰度、生物量较高, 其中春季远岸侧较高, 夏季近岸侧较高。分析其原因, 可能是相比保护区, 其附近海域临近象山港入海口, 夏季温度和光照条件适宜, 由于咸淡水交汇及生活用水排放, 存在赤潮发生的营养条件, 从而使微型藻类大量繁殖, 打破了保护区附近海域生态环境的稳定性(Feyrer et al, 2017; 刘旭东等, 2019); 此外保护区附近海域靠近陆地, 临近象山港入海口, 近岸与远岸的底部地质条件不同, 水深可能对海洋生物的分布有一定影响(Munga et al, 2013; Lange et al, 2014; Martins et al, 2017)。
3.3 群落干扰程度ABC曲线表明保护区与其附近海域均存在生物量累积曲线和丰度累积曲线相交的情况, 其中保护区附近海域夏季w为负值, 丰度累积曲线比生物量累积曲线面积更大(图 6), 由此可知夏季物种存在个体体型小型化(Warwick et al, 1994; Blanchard et al, 2004), 可能是由于夏季附近海域存在过度捕捞现象及人为条件下沉积物重金属污染造成(Gao et al, 2014; Handley et al, 2014), 说明夏季保护区附近海域群落结构受到了重度干扰状态。由夏季群落结构分析可知, 夏季保护区与附近海域完全分开, 表明夏季保护区和对照海域群落结构差异显著(图 5)。分析可知, 一方面由于保护区季节共有种多于其附近海域, 物种更替率小于其附近海域; 另一方面, 分析海域季节特征种情况发现, 春季特征种(保护区7种, 附近海域7种)大于夏季(保护区5种, 附近海域4种), 在特征种组成上, 春季包含节肢动物、软体动物、脊索动物、刺胞动物4门类, 而夏季附近海域特征种均为节肢动物, 特征种类群较为单一; 鉴于特征种对海域间物种组成影响显著(刘勇等, 2015; 张敬怀等, 2017), 因此单一类群的特征种组成及高物种更替率可能导致附近海域夏季干扰程度较大, 这也与ABC曲线的分析结果相吻合。
4 结论调查海域共出现海洋生物45属47种, 其中韭山列岛海洋生态自然保护区42种, 其附近海域37种。海洋生物以节肢动物门、软体动物门和脊索动物门的物种为主要组成部分, 其中节肢动物丰度和生物量最高; 日本鼓虾为保护区和其附近海域2季特征种, 保护区季节间物种更替率(64.29%)低于附近海域(72.97%); 保护区平均丰度为37.459ind/Agt, 平均生物量为59.160g/Agt, 其附近海域平均丰度为37.048ind/Agt, 平均生物量为37.230g/Agt, 保护区丰度和生物量高于其附近海域; 春季保护区与其附近海域多样性指数均较低, 夏季保护区多样性指数高于其附近海域; ABC曲线表明, 春季保护区及其附近海域处于轻微及未受到干扰状态, 夏季保护区处于轻微干扰状态, 其附近海域处于重度干扰状态。综上所述, 韭山列岛海洋生态自然保护区的设立, 在提高物种多样性、物种丰度、生物量及维持群落结构的稳定性方面优于保护区附近海域。
于鑫, 单秀娟, 李忠义, 等. 2017. 渤海底拖网主要渔业生物类别时空分布的初步研究. 南方水产科学, 13(2): 9-17 |
王金宝, 李新正, 王洪法. 2017. 山东宁津附近海域大型底栖动物群落结构及季节变化. 海洋与湖沼, 48(6): 1371-1382 |
中华人民共和国国家质量监督检验检疫总局, 2008a. GB/T 12763.6-2007海洋调查规范第6部分: 海洋生物调查.北京: 中国标准出版社, 1-157
|
中华人民共和国国家质量监督检验检疫总局, 2008b. GB/T 12763.9-2007海洋调查规范第9部分: 海洋生态调查指南.北京: 中国标准出版社, 1-20
|
邓小艳, 俞存根, 水玉跃, 等. 2018. 舟山近岸海域春秋季鱼类种类组成及其数量时空分布. 生态科学, 37(1): 10-19 |
卢衎尔, 朱文斌, 梁君, 等. 2019. 韭山列岛海域虾类群落结构与海洋环境因子的关系. 浙江大学学报(理学版), 46(1): 65-77 |
田甲申, 韩家波, 张明, 等. 2013. 大连斑海豹自然保护区海域渔业资源现状初步研究. 水产科学, 32(11): 646-652 |
曲慧敏, 王蕾, 邱盛尧, 等. 2017. 乳山近海渔业资源种类组成及变化. 水产科学, 36(3): 323-329 |
刘勇, 程家骅. 2015. 东海区底拖网作业三类主要渔获物的时空关系. 生态学报, 35(10): 3403-3410 |
刘旭东, 孙立娥, 张晓红, 等. 2019. 渤海海域夏季大型底栖动物群落特征. 中国环境监测, 35(3): 120-127 |
许友伟, 陈作志, 范江涛, 等. 2015. 南沙西南陆架海域底拖网渔获物组成及生物多样性. 南方水产科学, 11(5): 76-81 |
杜飞雁, 王雪辉, 贾晓平, 等. 2011. 大亚湾海域大型底栖生物种类组成及特征种. 中国水产科学, 18(4): 877-892 |
杜飞雁, 王雪辉, 贾晓平, 等. 2013. 大亚湾海域浮游动物种类组成和优势种的季节变化. 水产学报, 37(8): 1213-1219 |
张亮, 王尽文, 任荣珠, 等. 2014. 海洲湾北部海域春季渔业资源的群落结构特征. 渔业科学进展, 35(5): 1-7 |
张亚洲, 贺舟挺. 2013. 春、夏季韭山列岛海洋生态自然保护区海域渔业资源分析. 浙江海洋学院学报(自然科学版), 32(4): 292-298 |
张洪亮, 徐开达, 贺舟挺, 等. 2008. 韭山列岛附近海域渔业资源分析. 海洋渔业, 30(2): 105-113 |
张洪亮, 梁君, 贺舟挺, 等. 2012. 岱衢洋渔业动物多样性分析. 水生生物学报, 36(5): 922-931 |
张敬怀, 高阳, 时小军, 等. 2017. 大亚湾底拖网海洋生物种类组成及物种多样性. 生物多样性, 25(9): 1019-1030 |
贺舟挺, 张洪亮, 徐开达, 等. 2012. 韭山列岛自然保护区岩相潮间带底栖生物多样性与分布. 渔业信息与战略, 27(2): 151-156 |
徐开达, 卢衎尔, 卢占晖, 等. 2018. 韭山列岛自然保护区虾类优势种生态位. 生物多样性, 26(6): 601-610 |
Blanchard F, LeLoc'h F, Hily C et al, 2004. Fishing effects on diversity, size and community structure of the benthic invertebrate and fish megafauna on the Bay of Biscay coast of France. Marine Ecology Progress Series, 280: 249-260 |
Feyrer F, Slater S B, Portz D E et al, 2017. Pelagic nekton abundance and distribution in the northern Sacramento-San Joaquin Delta, California. Transactions of the American Fisheries Society, 146(1): 128-135 |
Flemming B W, 2000. A revised textural classification of gravel-free muddy sediments on the basis of ternary diagrams. Continental Shelf Research, 20(10-11): 1125-1137 |
Gao X L, Zhou F X, Chen C T A et al, 2014. Pollution status of the Bohai Sea: an overview of the environmental quality assessment related trace metals. Environment International, 62: 12-30 |
Handley S J, Willis T J, Cole R G et al, 2014. The importance of benchmarking habitat structure and composition for understanding the extent of fishing impacts in soft sediment ecosystems. Journal of Sea Research, 86: 58-68 |
Lange L, Griffiths C L, 2014. Large-scale spatial patterns within soft-bottom epibenthic invertebrate assemblages along the west coast of South Africa, based on the Nansen trawl survey. African Journal of Marine Science, 36(1): 111-124 |
Ludwig J A, Reynolds J F, 1988. Statistical Ecology. New York: John Wiley & Sons
|
Mace III M M, Kimball M E, Haffey E R, 2019. The nekton assemblage of salt marsh pools in a southeastern United States estuary. Estuaries and Coasts, 42(1): 264-273 |
Margalef R, 1958. Information theory in ecology. General Systems, 3(1): 36-71 |
Martins A S, Haimovici M, 2017. Seasonal mesoscale shifts of demersal nekton assemblages in the subtropical south-western Atlantic. Marine Biology Research, 13(1): 88-97 |
Munga C N, Mwangi S, Ong'anda H et al, 2013. Species composition, distribution patterns and population structure of penaeid shrimps in Malindi-Ungwana Bay, Kenya, based on experimental bottom trawl surveys. Fisheries Research, 147: 93-102 |
Pielou E C, 1975. Ecological Diversity. New York: John Wiley & Sons
|
Rizkalla S I, Akel E S H K, Ragheb E, 2016. Biodiversity and fisheries of the non-target catch from bottom trawl, off Alexandria, Mediterranean Sea, Egypt. Regional Studies in Marine Science, 3: 194-204 |
Song P Q, Lin L S, Li Y et al, 2016. Spatial structure and seasonal changes of nekton assemblages in the Taiwan Strait. Acta Oceanologica Sinica, 35(6): 59-67 |
Soykan O, Akgül ŞA, Kınacıgil H T, 2016. Catch composition and some other aspects of bottom trawl fishery in Siğacık Bay, central Aegean Sea, eastern Mediterranean. Journal of Applied Ichthyology, 32(3): 542-547 |
Stevenson D E, Lauth R R, 2019. Bottom trawl surveys in the northern Bering Sea indicate recent shifts in the distribution of marine species. Polar Biology, 42(2): 407-421 |
Warwick R M, 1986. A new method for detecting pollution effects on marine macrobenthic communities. Marine Biology, 92(4): 557-562 |
Warwick R M, Clarke K R, 1994. Relearning the ABC: taxonomic changes and abundance/biomass relationships in disturbed benthic communities. Marine Biology, 118(4): 739-744 |
 2020, Vol. 51
2020, Vol. 51


