中国海洋湖沼学会主办。
文章信息
- 陈晨, 焦海峰, 王一农, 刘懂, 孙元, 刘迅, 王莉, 陈启鹏. 2016.
- CHEN Chen, JIAO Hai-Feng, WANG Yi-Nong, LIU Dong, SUN Yuan, LIU Xun, WANG Li, CHEN Qi-Peng. 2016.
- 象山港海洋牧场示范区大型底栖生物的时空变化
- TEMPORAL AND SPATIAL CHANGES OF MACROBENTHOS IN MARINE PASTURE DEMONSTRATION AREA IN XIANGSHAN BAY
- 海洋与湖沼, 47(1): 130-139
- Oceanologia et Limnologia Sinica, 47(1): 130-139.
- http://dx.doi.org/10.11693/hyhz20151000254
-
文章历史
- 收稿日期: 2015-10-08
- 收修改稿日期: 2015-12-07
2. 宁波市海洋与渔业研究院 宁波 315012
2. Ningbo Academy of Oceanology and Fisheries, Ningbo 315012, China
海洋牧场(Marine Pasture)是指在某一海域内,采用一整套规模化的渔业设施和系统化的管理体制,利用自然的海洋生态环境,将人工增殖放流的经济海洋生物聚集起来,进行有计划有目的的海上放养鱼虾贝藻的大型人工渔场(Pickering et al,1999; 王亚民等,2011)。象山港在1990年代被定义为国家级“大鱼池”,但随着海洋资源的过度开发利用与人为污染,很多天然优良的海产养殖场的自然平衡遭到很大的破环,出现了富营养化甚至发生赤潮现象(翟滨等,2007; 曾相明等,2011)。为构建和谐的增养殖新模式,实现象山港的环境管理和水产养殖的可持续发展,改善象山港水域生态环境,保护渔业资源,宁波市制定了“象山港海洋牧场核心示范区建设”项目,2012年4月建设1个人工鱼礁群,形成鱼礁3.6×104m3; 移植大型海藻10 ha,放流各类鱼苗2.4×106尾。
大型底栖生物种类多、生活周期长、生活相对稳定(固着生活或做短距离移动),迁移能力低,对环境变化逃避能力弱,对水环境变化灵敏度高(Officer et al,1991; 尤仲杰等,2011a,b),因此是评价海洋牧场建设对渔业资源修复效果较佳的选择。本文通过对海洋牧场示范区建设前(2011年)、建设中(2012年)、建设后(2013年)为期3年的大型底栖生物时空变化的采集调查,比较分析海洋牧场建设前后大型底栖生物种类组成、数量分布、群落结构差异,探讨海洋牧场建设对象山港内生态环境的变化,为海洋牧场建设的修复效果评价提供较为完整的评价基础资料。
1 材料与方法 1.1 调查海域与站位分布象山港海洋牧场示范区位于白石山—中央山—铜山岛北侧、象山港航道以南600m海域,东北至白石山岛山嘴,西南至中央山北侧,东南到白石山沿岸,西北至象山港主航道南600m,海域面积4.2km2。本文分别在象山港全港海域和海洋牧场示范区及邻近区进行了大型底栖生物生态环境调查。
1.2 站位设置与采样时间设置图中S1—S5为海洋牧场示范区的调查站位,D1—D6为象山港全港区的调查站位,D1—D4为邻近区调查站位,具体调查站位分布见(图 1)。分别于海洋牧场示范区建设前(2011年4月、11月),建设中(2012年7月),建设后(2013年5月、11月)5个航次进行调查采集。
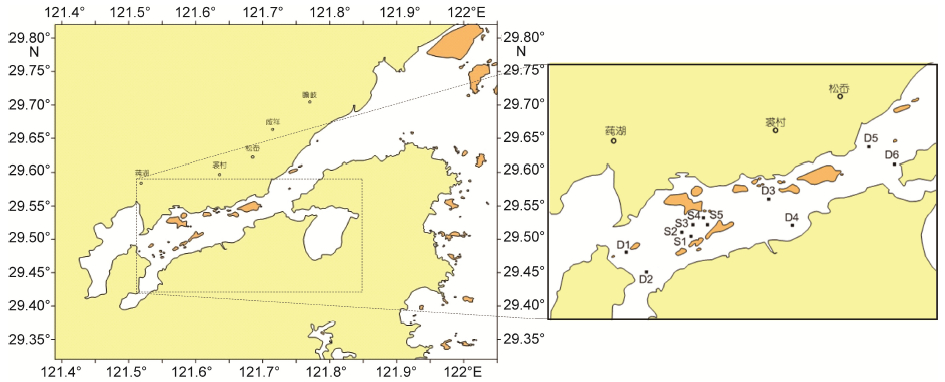 |
| 图 1 象山港海洋牧场示范区研究区域和调查站位 Fig. 1 Study area and sampling stations in the demonstration area of marine pasture in Xiangshan Bay |
海上采样、室内样本处理等工作按照《GB/T12763.6—2007.海洋调查规范》执行(中华人民共和国国家质量监督检疫总局,2007),所有样本的采集均使用0.05m2的HNM型抓斗式底质采泥器,每个站点重复采样3次,所获生物使用0.5mm孔径的网筛冲洗后用5%福尔马林现场固定,带回实验室进行种类鉴定、计数、称量与分析。
1.4 数据处理与分析优势度(Y)计算公式为Y=ni·fi/N,式中N为样本中的总个体数; ni为样本中第i种的个体数; fi为该种生物在样本中出现概率。优势种更替率(R)计算公式为R=(a+b-2c)/(a+b-c)·100%。a与b分别为相邻两个时期的优势种数,c为相邻两个时期共同的优势种数。
采用PRIMER5.0软件计算Shannon-Wiener多样性指数(H’)、Margalef物种丰富度指数(d)、Pielou均匀度指数(J),使用丰度/生物量比较法(ABC曲线)分析海域底栖生物群落结构稳定性; 利用PRIMER5.0对大型底栖生物的密度数据进行平方根转换,使用Bray-Curtis相似性等级聚类(CLUSTER)和非度量多维标度(nMDS)方法比较分析各个站位间群落结构的相似性。海洋牧场建设前后和调查区域的大型底栖生物群落比较,用软件提供的双因素相似性百分比(ANOSIM)分析,并运用相似性百分比(SIMPER)方法分别分析建设前后大型底栖生物群落内及群落间非相似性的关键贡献种。
采用SPSS19.0统计软件对大型底栖生物群落进行以建设前后变化和调查区域为因子的多因子方差分析,在作参数统计分析前,对数据进行正态检验(K-S检验)和方差齐次性检验(Levene’检验),显著性水平设置为α=0.05。使用Surfer 11.0软件作图。
2 结果与分析 2.1 种类组成与分布象山港海洋牧场示范区共获得大型底栖动物59种。其中软体动物有25种(42.37%)居首; 其次是多毛类15种(25.42%)、甲壳动物9种(15.25%)、棘皮动物6种(10.17%),其他类4种(6.78%),包括海葵(Anthopleura xanthogrammica)、白海箸(Virgularia gustaviana)、海豆芽(Lingula anatina)、六丝矛尾鰕虎鱼(Chaeturichthys hexanema)。
海洋牧场示范区大型底栖动物有34种,邻近区有33种,全港区有35种,示范区和邻近区共有47种,高于全港区,不同区域大型底栖动物组成情况见(图 2)。建设前后调查表明: 建设后获得的种类数最多,33种; 其次建设中29种; 建设前26种。各航次中软体动物种类数最多,是构成海洋牧场示范区大型底栖动物的主要类群,不同区域大型底栖动物建设前后变化情况见(图 3)。
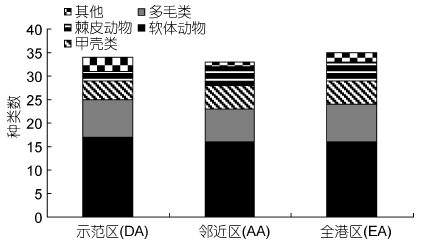 |
| 图 2 示范区(DA)、邻近区(AA)和全港区(EA)大型底栖生物的种类组成 Fig. 2 Composition of macrobenthic species in the demonstration area, the adjacent area, and the entire bay |
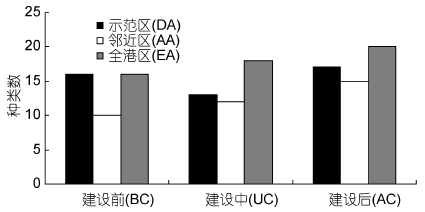 |
| 图 3 大型底栖生物建设前后种类数的变化 Fig. 3 Variation in species in the demonstration area, the adjacent area, and entire bay before and after the construction of marine pasture |
多因素方差分析结果表明: 海洋牧场建设前后大型底栖生物种类数差异极显著(F2,36=40.91,P<0.01),不同区域间无显著差异(F2,36=1.85,P=0.172)。
2.2 优势种海洋牧场示范区大型底栖生物的优势种类(Y≥0.02)(表 1)共有优势种13种,示范区(13种)>邻近区(12种)>全港区(8种),建设前(9种)>建设后(8种)>建设中(5种),建设中优势种减少。其中海洋牧场建设前不倒翁虫(Sternaspis scutata)的优势度最高,为0.11,建设中的半褶织纹螺(Nassarius semiplicata)的优势度最高,为0.19,建设后的薄倍棘蛇尾(Amphioplus praestans)的优势度最高,为0.17。
| 调查时间 | 优势种 | 调查区域 | ||
| 示范区 | 邻近区 | 全港区 | ||
| 建设前 | 不倒翁虫Sternaspis scutata | 0.11 | - | 0.04 |
| 巢沙蚕Diopatra amboinensis | - | 0.03 | - | |
| 纵肋织纹螺Nassarius variciferus | - | 0.07 | 0.08 | |
| 毛蚶Scapharca subcrenata | 0.04 | - | - | |
| 日本镜蛤Dosinorbis japonica | 0.05 | - | - | |
| 薄云母蛤Yoldia similis | - | 0.10 | 0.05 | |
| 端足类Amphipoda | - | 0.02 | - | |
| 薄倍棘蛇尾Amphioplus praestans | 0.03 | 0.08 | 0.05 | |
| 海豆芽Lingula anatina | 0.03 | - | - | |
| 建设中 | 半褶织纹螺Nassarius semiplicata | 0.19 | - | - |
| 纵肋织纹螺Nassarius variciferus | - | 0.03 | - | |
| 泥螺Bullacta exarata | - | 0.03 | - | |
| 婆罗囊螺Retusa borneensis | - | 0.03 | - | |
| 薄倍棘蛇尾Amphioplus praestans | - | - | 0.06 | |
| 建设后 | 不倒翁虫Sternaspis scutata | 0.02 | 0.02 | - |
| 巢沙蚕Diopatra amboinensis | 0.07 | - | 0.03 | |
| 异足索沙蚕Lumbricomereis heeropoda | 0.05 | - | - | |
| 纵肋织纹螺Nassarius variciferus | 0.05 | - | - | |
| 双带光螺Melanella bivittata | 0.09 | - | - | |
| 日本镜蛤Dosinorbis japonica | 0.03 | 0.04 | - | |
| 薄云母蛤Yoldia similis | 0.13 | 0.04 | 0.04 | |
| 薄倍棘蛇尾Amphioplus praestans | - | 0.17 | 0.14 | |
| “-”表示该区域大型底栖生物Y<0.02未成优势种 | ||||
建设前和建设后共有种为6种,建设中和建设前、建设后共有种为2种,薄倍棘蛇尾(Amphioplus praestans)、纵肋织纹螺(Nassarius variciferus)在3个时期均有出现。建设前和建设中种类更替率达83.3%,建设中和建设后种类更替率达81.8%,优势种类更替变化明显。
2.3 栖息密度和生物量年平均栖息密度与生物量建设前后变化情况,示范区(109.83 ind/m2)>全港区(99.43 ind/m2)>邻近区(91.67 ind/m2); 示范区(28.10 g/m2)>邻近区(21.93 g/m2)>全港区(19.92 g/m2)(图 4)。建设前(150.83 ind/m2)>建设中(78.67 ind/m2)>建设后(71.43 ind/m2); 建设中(32.18 g/m2)>建设后(23.27 g/m2)>建设前(14.50 g/m2)(图 5)。
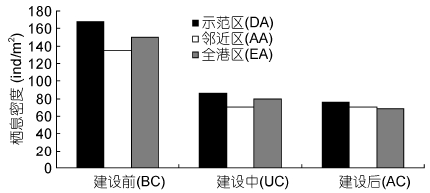 |
| 图 4 大型底栖生物栖息密度 Fig. 4 Density of macrobenthos in the demonstration area, the adjacent area, and the entire bay |
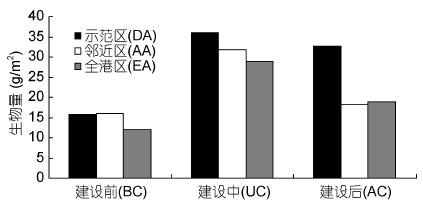 |
| 图 5 大型底栖生物生物量 Fig. 5 Biomass of macrobenthos in the demonstration area, the adjacent area, and the entire bay |
多因素方差分析结果表明: 大型底栖生物栖息密度海洋牧场建设前后存在极显著差异(F2,36=11.23,P<0.01),不同区域间无显著差异(F2,36=2.25,P=1.20); 生物量建设前后(F2,36=1.81,P=0.178)和不同区域间(F2,36=1.56,P=0.224)均无显著差异。
2.4 生物多样性指数象山港调查区域大型底栖生物群落生物多样性指数在海洋牧场建设前后变化情况见图 6。按区域划分多样性指数H’、丰富度指数d、均匀度指数J均为: 邻近区>全港区>示范区; 按建设前后划分: 除均匀度指数J外,多样性指数H’、丰富度指数d均表现为: 建设前>建设后>建设中,均匀度指数则表现为建设中>建设后>建设前,建设后大型底栖生物群落个体数量在不同种类中分布趋于均匀。
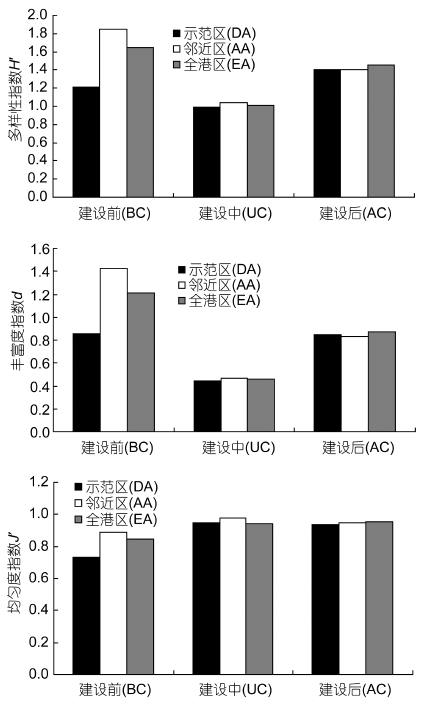 |
| 图 6 大型底栖生物群落生物多样性指数 Fig. 6 Biodiversity indices of macrobenthic communities in demonstration area, the adjacent area, and the entire bay |
多因素方差分析结果表明: 大型底栖生物在海洋牧场建设前后多样性指数H’(F2,36 =15.67,P<0.01),丰富度指数d(F2,36=34.71,P<0.01),均匀度指数 J(F2,36=11.66,P<0.01),均存在极显著差异; 不同区域间,多样性指数H’(F2,36=1.68,P=0.201),丰富度指数d(F2,36=1.77,P=0.185),均匀度指数J(F2,36=1.74,P=0.190)均无显著差异(P>0.05)。
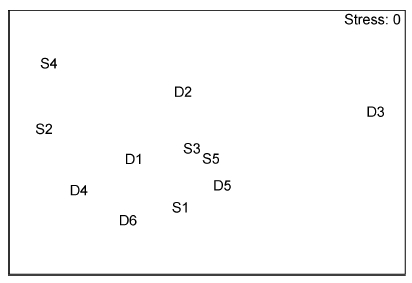
2.5 群落结构群落聚类及nMDS排序分析结果表明,海洋牧场建设前后大型底栖生物群落组成存在明显差异(图 7—图 12)。建设前,有6个站点相似性超过40%,建设中,无站点相似性超过40%,建设后,有4个站点相似性超过40%。示范区、邻近区、全港区的各个站点分布均较离散,说明相似度较低。
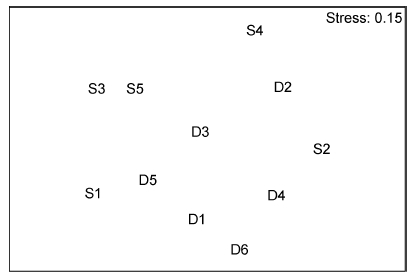 |
| 图 7 海洋牧场建设前大型底栖生物群落的nMDS排序 Fig. 7 The nMDS plots for macrobenthic communities before the construction |
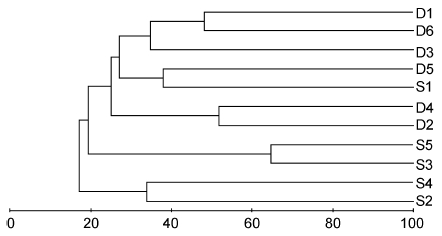 |
| 图 8 海洋牧场建设前大型底栖生物群落树状聚类图 Fig. 8 The dendrogram for the CLUSTER of macrobenthic communities before the construction |
 |
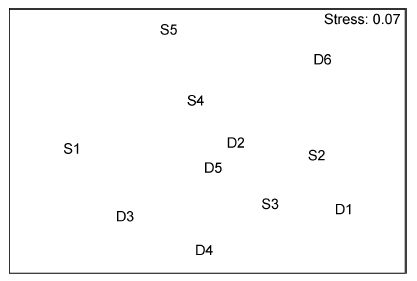
| 图 9 海洋牧场建设中大型底栖生物群落的nMDS排序 Fig. 9 The nMDS plots for macrobenthic communities during the construction |
 |
| 图 10 海洋牧场建设中大型底栖生物群落树状聚类图 Fig. 10 The dendrogram for the CLUSTER of macrobenthic communities during the construction |
 |
| 图 11 海洋牧场建设后大型底栖生物群落的nMDS排序 Fig. 11 The nMDS plots for macrobenthic communities after the construction |
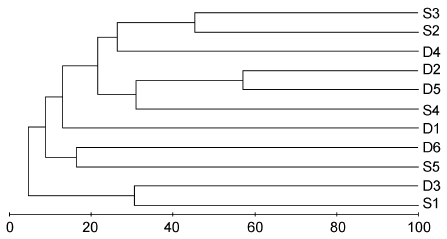 |
| 图 12 海洋牧场建设后大型底栖生物群落树状聚类图 Fig. 12 The dendrogram for the CLUSTER of macrobenthic communities after the construction |
双因素相似性分析(ANOSIM)结果表明,大型底栖生物群落建设前后存在显著性差异(综合检验R=0.215,P=0.004),区域间无显著性差异(R=0.034,P=0.347)。建设前后两两检验结果见(表 2)。
| 组别 | 综合检验R | 成对检验R | P |
| 建设前后 | 0.215 | - | 0.004 |
| 区域间 | 0.034 | - | 0.347 |
| 建设前vs建设中 | - | 0.264 | 0.006 |
| 建设前vs建设后 | - | 0.26 | 0.008 |
| 建设中vs建设后 | - | 0.187 | 0.035 |
根据SIMPER分析结果见(表 3、表 4),建设前大型底栖生物群落的平均相似性为17.57%,其中,群落最大贡献者为纵肋织纹螺(26.02%),其次为薄倍棘蛇尾(15.93%); 建设中大型底栖生物群落的平均相似性为7.14%,最大贡献者为半褶织纹螺(73.45%),其次为薄倍棘蛇尾(11.32%),半褶织纹螺占绝对的优势地位; 建设后的群落的平均相似性为11.51%,最大贡献者为薄云母蛤(29.97%),其次为日本镜蛤(18.88%),软体动物一直在数量上占据优势,并且随着时间的推移软体动物所占贡献种比例逐渐升高。建设前和建设中大型底栖生物群落间的平均非相似性为94.89%,薄倍棘蛇尾、半褶织纹螺、纵肋织纹螺、不倒翁虫为造成群落间差异的重要贡献物种; 建设前和建设后大型底栖生物群落间的平均非相似性为88.74%,薄倍棘蛇尾、不倒翁虫、纵肋织纹螺、薄云母蛤、毛蚶、日本镜蛤、巢沙蚕为造成群落间差异的重要贡献物种; 建设中和建设后大型底栖生物群落间的平均非相似性为96.10%,半褶织纹螺、薄倍棘蛇尾、薄云母蛤、纵肋织纹螺、异足索沙蚕为造成群落间差异的重要贡献物种。
| 种类 | 贡献率(%) | |||
| 建设前 | 建设中 | 建设后 | ||
| 纵肋织纹螺 | Nassarius variciferus | 26.02 | - | 13.11 |
| 薄倍棘蛇尾 | Amphioplus praestans | 15.93 | 11.32 | - |
| 薄云母蛤 | Yoldia similis | 10.57 | - | 29.97 |
| 半褶织纹螺 | Nassarius semiplicata | - | 73.45 | - |
| 日本镜蛤 | Dosinorbis japonica | - | - | 18.88 |
| 异足索沙蚕 | Lumbricomereis heeropoda | - | - | 15.13 |
| *SIMPER分析, 依次列出贡献率达到10%以上的重要物种 | ||||
| 平均非相似性(%) | 种类 | 贡献率(%) | ||
| 建设前vs建设中 | 94.89 | 薄倍棘蛇尾 | Amphioplus praestans | 11.07 |
| 半褶织纹螺 | Nassarius semiplicata | 9.66 | ||
| 纵肋织纹螺 | Nassarius variciferus | 8.83 | ||
| 不倒翁虫 | Sternaspis scutata | 6.70 | ||
| 建设前vs建设后 | 88.74 | 薄倍棘蛇尾 | Amphioplus praestans | 8.72 |
| 不倒翁虫 | Sternaspis scutata | 8.46 | ||
| 纵肋织纹螺 | Nassarius variciferus | 7.43 | ||
| 薄云母蛤 | Yoldia similis | 7.28 | ||
| 毛蚶 | Scapharca subcrenata | 5.94 | ||
| 日本镜蛤 | Dosinorbis japonica | 5.33 | ||
| 巢沙蚕 | Diopatra amboinensis | 5.09 | ||
| 建设中vs建设后 | 96.10 | 半褶织纹螺 | Nassarius semiplicata | 9.28 |
| 薄倍棘蛇尾 | Amphioplus praestans | 9.24 | ||
| 薄云母蛤 | Yoldia similis | 6.62 | ||
| 纵肋织纹螺 | Nassarius variciferus | 5.84 | ||
| 异足索沙蚕 | Lumbricomereis heeropoda | 5.15 | ||
| *SIMPER分析, 仅列出贡献率达到5%以上的重要物种 | ||||
丰度/生物量比较曲线(ABC曲线),从中可以看出,建设前丰度曲线始终位于生物量曲线之上(图 13),说明大型底栖生物群落结构在建设前未受到明显的扰动; 建设中大型底栖生物丰度与生物量曲线出现了明显的交叉现象(图 14),表明建设中大型底栖生物收到了强烈的干扰,人工鱼礁投放后会对其周围海域产生影响,建设后未出现明显的扰动(图 15),表明随着时间的推移,海洋牧场建设过程中带来的扰动逐渐减小,并围绕鱼礁逐渐形成新的人工生态系统。
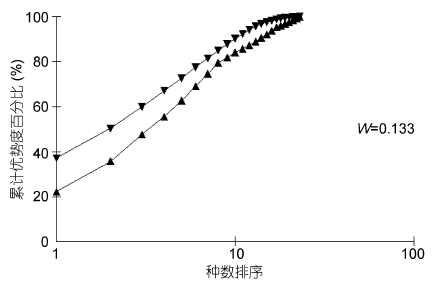 |
| 图 13 海洋牧场建设前大型底栖生物丰度/生物量比较曲线 Fig. 13 ABC plots of macrobenthos before the construction of marine pasture in Xiangshan Bay |
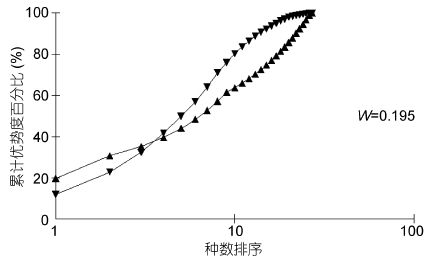 |
| 图 14 海洋牧场建设中大型底栖生物丰度/生物量比较曲线 Fig. 14 ABC plots of macrobenthos during the construction of marine pasture in Xiangshan Bay |
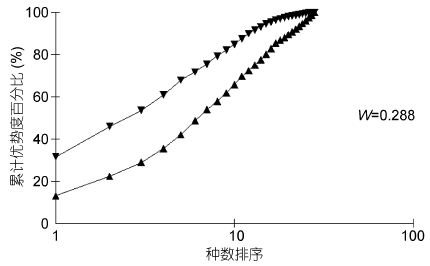 |
| 图 15 海洋牧场建设后大型底栖生物丰度/生物量比较曲线 Fig. 15 ABC plots of macrobenthos after the construction of marine pasture in Xiangshan Bay |
通过对象山港海洋牧场示范区建设前(2011年)、建设中(2012年)、建设后(2013年)连续3年大型底栖生物调查结果分析可知:(1)种类数随着海洋牧场的建设完善而增加,建设过程中优势种的更替率均>80%,表明建设后主要组成种类发生了显著变化,同时多样性指数建设前后呈现显著差异,均匀度指数建设后高于建设前,说明象山港海洋牧场建设使底栖生态环境发生较大变化,有利于大型底栖生物群落结构的稳定性,与斯广杰等(2010)结论一致。(2)海洋牧场建设过程中,平均栖息密度随着海洋牧场建设而降低,平均生物量在建设中呈现最高,建设后其次,建设前最低,生物数量变化受到示范区建设影响明显。其中,示范区的栖息密度和生物量在建设中、建设后一直高于邻近区和全港区,表明海洋牧场建设有利于示范区生物数量增长。(3)群落聚类分析表明,建设前,有6个站点相似性超过40%,建设中无站点相似性超过40%,建设后,有4个站点相似性超过40%; 同时根据SIMPER分析结果,建设前后生物群落平均相似性为建设前(17.57%)>建设后(11.51%)>建设中(7.14%),建设中半褶织纹螺贡献率达73.45%,占绝对的优势地位,使群落数量组成单一。以上结论相符,都表明建设中各个站点群落相似度最低,这与人工投礁过程中海底部受到影响有关,改变了示范区部分的生态环境,不同的生境栖息着不同结构的底栖生物群落,导致建设中的各个站点群落结构存在着差异,群落相似度低(顾晓英等,2010; Giulio et al,1994)。
与历史数据相比较,象山港大型底栖生物在种类数、栖息密度、生物量、多样性指数均发生了较大的变化(顾晓英等,2010; 廖一波等,2011,2014),由于历史数据的调查时间和站位不同,不能直接比较,但仍能得出: 种类数、栖息密度、生物量呈现减少的趋势,这可能与后期象山港沿岸围塘养殖面积不断扩大和海水养殖业的迅猛发展有关,使底栖生物的栖息地范围变小,大型底栖生物种类数量日益减少(王金辉等,2006; 尤仲杰等,2011a,b; 周伟男等,2013)。但是海洋牧场示范区建设后种类数、生物量、多样性指数均高于建设前,并且海洋牧场示范区及其邻近区的种类数、栖息密度、生物量均高于全港区(表 5),说明海洋牧场建设有利于示范区大型底栖生物改善,这和其他关于海洋牧场中人工鱼礁建设改善生物生态效果的研究结果相似,海洋牧场的建设对生态的修复是有益的(Ambrose et al,1990; 张虎等,2008; 程飞等,2014)。
3.2 海洋牧场示范区建设效果评价海洋牧场是一项改善和修复海洋生态环境,增值和保护渔业资源的公益性事业,影响到的海洋生物包括底栖生物、浮游植物、浮游动物,但是建设以后能否产生显著效益,关键在于海洋牧场建设是否合理、完善(陶峰等,2009)。宁波市政府于2008年就曾在白石山海域投放230个水泥鱼礁体(共5000m3)以作为前期试验(宁波市海洋与渔业局,2009)。廖一波等(2014)于2010年(4季)对2008年投礁的象山港人工鱼礁及其邻近海域进行大型底栖生物调查,研究发现人工鱼礁区的大型底栖生物平均密度、生物量、多样性指数均显著高于全港区,说明人工鱼礁的投放为大型底栖生物提供良好的栖息环境。江志兵等(2012)于2010年(4季)对2008年投礁的象山港人工鱼礁及其邻近海域网采浮游植物结果表明,人工鱼礁投放对网采浮游植物群落无显著影响,但显著高于2006—2007年和2006—2009年(尤仲杰等,2011a,b),可见人工鱼礁投放后白石山及其邻近海域浮游植物丰度较投放前有明显升高,且随时间积累,人工鱼礁对其影响越趋显著。
本次调查的海洋牧场核心示范区,是在之前人工鱼礁投放的基础上,完善了海洋牧场示范区建设。陈海峰等(2013年)、陈涛等(2013)在和本文相同的(2012年4月投礁)投礁海域于2011年7(建设前)月2012年7月(建设中)在象山港人工鱼礁海域进行网采浮游植物和浮游动物调查,其中浮游植物投礁后生态指数和丰度鱼礁区都略高对照区,浮游动物投礁后,生物量、丰度等鱼礁区与对照区相比也相对较高,鱼礁区及其附近海域环境较对照区的更适合浮游生物群落生长与繁殖。结合本次历时3年的调查,建设后海洋牧场示范区的大型底栖生物平均密度、生物量均显著高于全港区,多样性指数在建设前示范区的和邻近区和全港区相差很大,建设后差距变小了,这都说明象山港海洋牧场已经开始发挥其良好的作用。通过总结象山港多年调查得到的大型底栖生物、浮游植物、浮游动物等文章都表明象山港的海洋牧场建设合理,并且随着进一步的完善,生态修复效果更加明显。
3.3 海洋牧场示范区建设对群落稳定性的影响大型底栖生物生活相对稳定,对海洋环境变化灵敏(Resh et al,1995),Warwick(1986)提出丰度/生物量比较曲线(ABC曲线)可以就由干扰造成的大型底栖生物群落变化做出灵敏的反应(Craeymeersch,1991; Dauer et al,1993; 李宝泉等,2007)。象山港海洋牧场示范区调查站位的数据作出的ABC曲线,在建设前不交叉、不重叠、不翻转,建设中丰度与生物量曲线出现明显交叉,建设后又呈现不交叉、不重叠、不翻转的现象。同时海洋牧场建设前后大型底栖生物的种类数、栖息密度、多样性指数、丰富度指数、均匀度指数、群落结构均有显著性差异或极显著差异,说明海洋牧场建设影响大,建设前后群落发生了较大的变化,丰富度指数、多样性指数均是建设前>建设后>建设中,在建设中出现最低值,建设后又增加。上述结果均表明该区域在建设前大型底栖生物群落处于一个相对稳定的状态,海洋牧场建设过程中改变了大型底栖生物的生态环境,使得大型底栖生物群落出现一定的扰动,但是在建设后扰动消失,同时种类及生物量建设后均高于建设前,说明群落系统拥有自我恢复能力,在人工鱼礁投放、大型藻类移植、鱼苗放流结束后一段时间,建设示范区的大型底栖生物资源会有所增加,并恢复到一个新的稳定状态,从而达到改善底栖生物环境的效果,这与相关研究的结果相似(张虎等,2008; 斯广杰等,2010)。分析出现波动的原因,(1)在海洋牧场示范区建设过程中,鱼礁的投放等的一些活动破坏了原海域水环境和底质环境的生态平衡,干扰了大型底栖生物的繁殖和生存,使靠近鱼礁的示范区的生物多样性降低,但是建设后,因人工鱼礁的投放使得原本的粉砂质粘土的底质拥有了礁岩性质的生境,会吸引和诱集礁岩性质的底栖生物在此栖息、产卵和庇护,使得底栖生物的种类不断增加,并且随着时间的推移,形成了新的人工生态系统(Rhoads,1970; 秦传新等,2011; 孙习武等,2011)。(2)海洋牧场建设后,示范区的上层水面养殖大型海藻,增加浮力的浮标布满了整个水面,直接影响了船只的行走、人为的捕捞,形成了保护区域,使得底栖生物受到人为捕捞的影响大大降低,与建设前该区域和建设后其他区域产生差异,但目前还没有相关文献报道证明这一猜测,还有待进一步研究确认。
| 王亚民,郭冬青,2011.我国海洋牧场的设计与建设.中国水产, (4):25-27 |
| 王金辉,杨春旺,孙亚伟等,2006.象山港大型底栖动物的生物多样性和次级生产力研究.天津农学院学报, 13(2):24-28 |
| 尤仲杰,陶磊,焦海峰等,2011a.象山港大型底栖动物功能群研究.海洋与湖沼, 42(3):432-435 |
| 尤仲杰,焦海峰,2011b.象山港生态环境保护与修复技术研究.北京:海洋出版社, 217-221 |
| 中华人民共和国国家质量监督检疫总局,2007.海洋调查规范GB/T 12763.6-2007.北京:中国标准出版社, 41-44 |
| 宁波市海洋与渔业局,2009. 2008年宁波市海洋环境公报, 27 |
| 江志兵,陈全震,寿鹿等,2012.象山港人工鱼礁区的网采浮游植物群落组成及其与环境因子的关系.生态学报, 32(18):5813-5824 |
| 孙习武,孙满昌,张硕等,2011.海州湾人工鱼礁二期工程海域大型底栖生物初步研究.生物学杂志, 28(1):57-61 |
| 李宝泉,李新正,王洪法等,2007.长江口附近海域大型底栖动物群落特征.动物学报, 53(1):76-82 |
| 张虎,刘培廷,汤建华等,2008.海州湾人工鱼礁大型底栖生物调查.海洋渔业, 30(2):97-104 |
| 陈涛,廖勇,王云龙等,2013.象山港人工鱼礁海域浮游动物群落生态变化.海洋通报, 32(6):710-716 |
| 陈海峰,王云龙,廖勇等,2013.象山港人工鱼礁区浮游植物群落特征.海洋渔业, 35(4):396-404 |
| 周伟男,孙省利,李荣冠等,2013.湛江湾大型底栖动物的群落结构和多样性特征.广东海洋大学学报, 33(1):1-8 |
| 秦传新,陈丕茂,贾晓平,2011.人工鱼礁构建对海洋生态系统服务价值的影响——以深圳杨梅坑人工鱼礁区为例.应用生态学报, 22(8):2160-2166 |
| 顾晓英,陶磊,尤仲杰等,2010.象山港大型底栖动物群落特征.海洋与湖沼, 41(2):208-213 |
| 陶峰,贾晓平,陈丕茂等,2009.广东省澄海莱芜拟建礁区建礁可行性研究.安徽农业科学, 37(18):8608-8611 |
| 斯广杰,陈丕茂,杜飞雁等,2010.深圳杨梅坑人工鱼礁区投礁前后大型底栖动物种类组成的变化.大连海洋大学学报, 25(3):243-247 |
| 程飞,纪雅宁,李倨莹等,2014.象山港海湾生态系统服务价值评估.应用海洋学学报, 33(2):222-228 |
| 曾相明,管卫兵,潘冲,2011.象山港多年围填海工程对水动力影响的累积效应.海洋学研究, 29(1):73-83 |
| 廖一波,寿鹿,曾江宁等,2011.象山港不同养殖类型海域大型底栖动物群落比较研究.生态学报, 31(3):646-653 |
| 廖一波,曾江宁,寿鹿等,2014.象山港人工鱼礁投放对大型底栖动物群落结构的影响.海洋与湖沼, 45(3):487-495 |
| 翟滨,曹志敏,蓝东兆等,2007.象山港养殖海域水体和沉积物中营养元素的分布特征及其控制过程的初步研究.海洋湖沼通报, (3):49-56 |
| Ambrose R F, Anderson T W,1990. Influence of an artificial reef on the surrounding infaunal community. Marine Biology, 107(1):41-52 |
| Craeymeersch J A,1991. Applicability of the abundance/biomass comparison method to detect pollution effects on intertidal macrobenthic communities. Hydrobiological Bulletin, 24(2):133-140 |
| Dauer D M, Luckenbach M W, Rodi Jr A J,1993. Abundance biomass comparison (ABC method):effects of an estuarine gradient, anoxic/hypoxic events and contaminated sediments. Marine Biology, 116(3):507-518 |
| Giulio R, Nadia Z, Francesca T et al,1994. Patterns of sessile macrobenthos community development on an artificial reef in the Gulf of Genoa (northwestern Mediterranean). Bulletin of Marine Science, 55(2-3):745-771 |
| Officer C B, Smayda T J, Mann R,1991. Benthic filter feeding:a natural eutrophication control. Marine Ecology Progress Series, 69:178-188 |
| Pickering H, Whitmarsh D, Jensen A,1999. Artificial reefs as a tool to aid rehabilitation of coastal ecosystems:investigating the potential. Marine Pollution Bulletin, 37(8-12):505-514 |
| Resh V H, Norris R H, Barbour M T,1995. Design and implementation of rapid assessment approaches for water resource monitoring using benthic macroinvertebrates. Australian Journal of Ecology, 20(1):108-121 |
| Rhoads, D C,1970. Mass properties, stability and ecology of marine muds related to burrow activity. In:Crimes T P, Harper J C eds. Trace Fossils. Liverpool:Seel House Press, 391-460 |
| Warwick R W,1986. A new method for detecting pollution effects on marine macrobenthic communities. Marine Biology, 92(4):557-562 |
 2016, Vol. 47
2016, Vol. 47


