中国海洋湖沼学会主办。
文章信息
- 李玉, 高焕, 刘付程. 2016.
- LI Yu, GAO Huan, LIU Fu-Cheng. 2016.
- 海水养殖池沉积物中重金属形态和生物酶活性的关系研究
- CORRELATION BETWEEN SPECIATION OF HEAVY METAL AND ENZYMATIC ACTIVITY IN SURFACE SEDIMENT OF MARICULTURE POND
- 海洋与湖沼, 47(1): 83-90
- Oceanologia et Limnologia Sinica, 47(1): 83-90.
- http://dx.doi.org/10.11693/hyhz20150400108
-
文章历史
- 收稿日期: 2015-04-10
- 收修改稿日期: 2015-08-10
生物酶可催化各种反应过程,对土壤的微生物生态具有重要作用,因此土壤的酶活性被广泛当作土壤健康的生物指示物(Dick,1997)。土壤中微生物是各种酶的重要来源,微生物数量随土壤类型不同而存在很大的差异,主要受到土壤质量状况及土壤中有毒重金属及类金属污染的影响。如重金属As对所有细菌都具毒性,它能够阻止基础细胞的能量代谢功能,由于砷化合物的污染,土壤中微生物种群下降已经得到证实(Hiroki,1993;Walker et al,2000;Lorenz et al,2006)。在海洋环境中,由于对生态功能有直接且持续的负面冲击,重金属对沉积物中微生物群落多样性和动力过程的影响研究时有报道(Valsecchi et al,1995),最常见的就是降低胞外酶的活性(Li et al,2006;De Souza et al,2006;Wang et al,2007),如Cd、Zn、Ni、Co对细菌的一氧化二氮还原酶有抑制作用,从而导致温室气体的累积(Sobolev et al,2008;Haferburg et al,2010)。这些研究表明,海洋沉积物中重金属元素和酶活性有一定的关系。多年来研究者对近海海洋沉积物中重金属的富集状况、评价方法以及对生态的潜在危害进行了大量报道(Wang et al,2011;Choi et al,2012;Zhu et al,2012;Ho et al,2013;Zhang et al,2013),如何找到一个敏感的生物指标来判断无机重金属污染过程是一个亟待解决的问题。有研究者对河口、河道沉积物及农田、矿区土壤中生物酶的活性变化及与重金属的相关关系进行了初步探讨(Gianfreda et al,2005;Kavamura et al,2010;Colin et al,2012;Sivakumar et al,2012),近两年来又有研究者对北美、欧洲及荷兰不同利用功能的土壤中生物酶活性进行了测定(Talbot et al,2014;Hendriksen et al,2016;Rutgers et al,2016),也有研究者试验了环境因子对土壤中生物酶活性的稳定作用以抵抗外来胁迫(Elzobair et al,2016;Hu et al,2016)。刘存歧等(2007)报道了长江口潮滩湿地沉积物中生物酶活性和环境因子的相关性;Yu等(2001)研究表明缺氧环境下的河流沉积物中Cu、Cd和Pb对脲酶、转化酶、碱性磷酸酶和蛋白酶有明显的抑制作用,而Cr对生物酶则具有激活作用;史长青(1995)对稻田土壤中酶活性与重金属含量进行了相关性分析,发现脲酶活性与Cd、Cu、Zn、过氧化氢酶活性与Pb皆呈显著负相关关系;Ghosh等(2004)发现砷长期污染对微生物脱氢酶的活性产生不利影响。但当重金属总量对土壤中生物酶活性影响不显著的时候,重金属的某一赋存形态却能显著影响生物酶活性(刘云国等,2002)。运用连续提取法研究土壤重金属的赋存形态,可以了解土壤中重金属的转化和迁移,还可以预测其生物可利用性,更加客观地评价重金属的环境效应(Tessier et al,1979;Rauret,1998)。刘霞等(2002,2003)、蔡信德等(2005)研究了土壤中重金属形态和特定酶活性的关系,结果表明酶的活性和重金属在土壤中的迁移转化过程相关,说明以重金属的赋存形态来分析重金属对生物酶活性的影响比用总量更为准确。
本研究以连云港市海水养殖池表层沉积物中重金属赋存形态和生物酶活性为研究对象,通过对二者关系的探讨,旨在建立一种利用生物酶活性来指示沉积环境中重金属的生物可利用度和形态转化过程的判断方法。近海环境中,不同功能区沉积物中重金属形态及环境特点不同(Zhang et al,2012;王小静等,2015)。在海水养殖池这样一个相对封闭的环境中,受长期累积的影响,一旦发生重金属污染将直接影响养殖质量,进而影响人类健康。有研究者对养殖区海水水质、沉积物中异养细菌生态分布及沉积物酶活性和微生物群落结构分布进行了报道(李越蜀等,2012;宋科等,2013;廖红芳等,2014)。相对于实验室内设定或特定环境中高浓度的重金属对酶活性的影响研究,对养殖环境质量问题的探讨更具现实意义,但是对于封闭的海水养殖池塘多种重金属复合污染情况下重金属元素不同赋存形态间的迁移转化与酶活性的响应关系尚无系统的研究报道。
1 材料与方法 1.1 站点设置2014年9月在连云港赣榆县海头镇、九里镇、宋庄镇海水养殖区设置采样点9个,见图 1。海头镇位于连云港赣榆区东北部,海岸线长约11.6km,盛产各种海鲜,尤以黄鱼、梭子蟹、东方对虾、紫菜、贝类等海鲜珍品为最,是连云港市“海淡水养殖之乡”;人口8.2万,工业发展突出。九里镇位于连云港市赣榆区东北部,与山东省日照市接壤,东部沿海建有浅海域圈护养基地、潮间带滩涂贝类和紫菜养殖基地以及潮上带梭子蟹养殖基地;人口7万,以农业为主。宋庄镇紧靠赣榆城区,赣榆区经济开发区坐落境内,是全国“对虾养殖之乡”;工农业发展基本持平,人口2.6万,主要经济活动围绕养殖产业,如连云港人工鱼礁工程、全国首家海水养殖有机食品基地、工厂化养殖等。每个养殖池采样点周边环境相似,主要污染来源为工业农业废水和城镇生活污水,养殖品种皆为对虾。根据对角线法每个采样点采集5个样品,每个样品各取表层沉积物约100g,5个样品等量充分混合装入封口袋。
 |
| 图 1 调查站位 Fig. 1 Sampling stations |
采集的样品分成两份,一份用于检测重金属的赋存形态,预处理方法见《海洋监测规范》,本实验采用Tessier等(1979)连续提取法进行沉积物中重金属元素的赋存形态分离,重金属的形态可分为5种:可交换态(Ⅰ)、碳酸盐结合态(Ⅱ)、铁锰氧化物态(Ⅲ)、有机-硫化物态(Ⅳ)、残渣态(Ⅴ)。采用等离子体发射光谱仪测定赋存形态的含量。另一份样品用于土壤酶活性的测定。实验室内将采集的沉积物样品自然风干,玛瑙研钵研磨、过160目筛,样品采集两周内进行生物酶活性测定,测定方法:过氧化氢酶采用高锰酸钾滴定法;转化酶(蔗糖酶)采用3,5-二硝基水杨酸比色法;脲酶采用苯酚一次氯酸钠比色法;碱性磷酸酶采用改进后的磷酸苯二钠比色法(关松荫,1986;赵兰坡等,1986)。
1.3 数据分析利用SPSS 20.0统计软件进行显著性及相关性分析。
2 结果 2.1 养殖池表层沉积物中重金属赋存形态现状评价连云港临海养殖池表层沉积物中7种重金属元素Cu、Zn、Pb、Cd、Cr、As、Mn的赋存形态分析结果参见图 2。就5种赋存形态而言,可交换态浓度所占百分比最高的是Cd;碳酸盐结合态较高的是Mn、Pb和Cd;铁锰氧化物态最高的是Pb、Mn、Zn;有机结合态最高的是Cu、Zn;残渣态最高的是Cr和As。
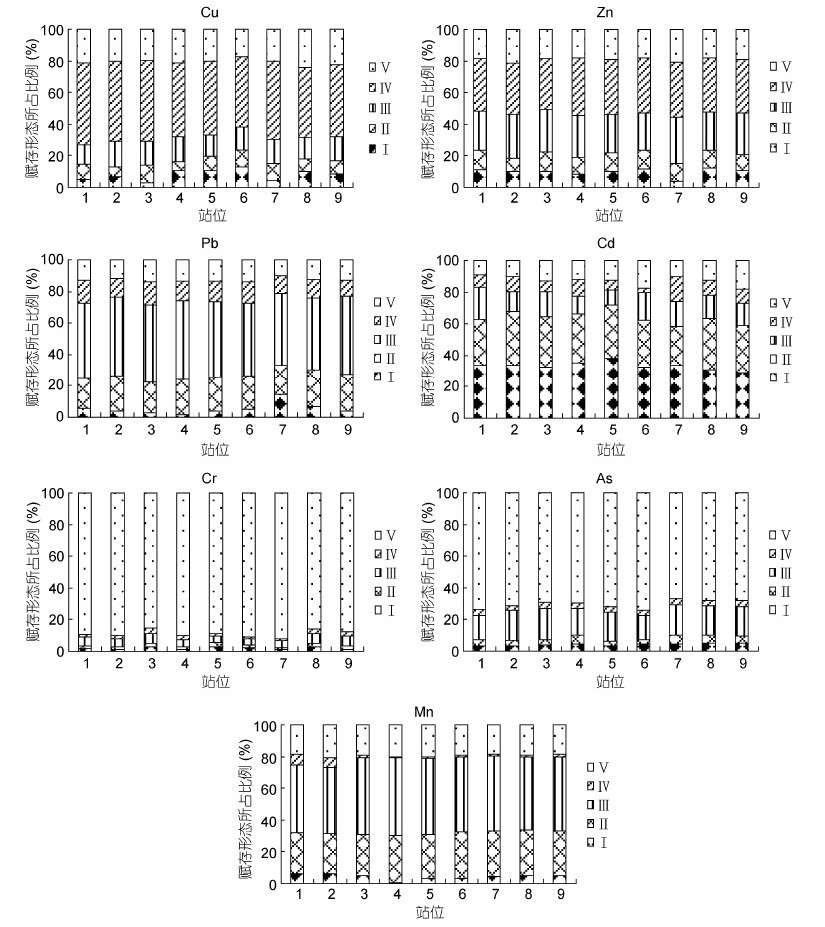 |
| 图 2 沉积物中重金属赋存形态的分布 Fig. 2 Distribution of different forms ofheavy metals in sediments Ⅰ可交换态,Ⅱ碳酸盐结合态,Ⅲ铁锰氧化物态,Ⅳ有机-硫化物态,Ⅴ残渣态 |
本次调查活动设置的9个站点表层沉积物中脲酶、碱性磷酸酶、过氧化氢酶、转化酶的活性见表 1。脲酶的活性范围为0.45—8.96mg/(g∙24h),存在明显的空间差异性;碱性磷酸酶活性范围为2.45— 6.69mg/(g∙24h),过氧化氢酶活性范围为0.14— 2.36mL/(g∙24h),空间分布较为均匀;转化酶活性范围为0.45—10.45mg/(g∙24h),空间差异性大。
| 站位 | 脲酶[mg/(g∙24h)] | 碱性磷酸酶[mg/(g∙24h)] | 过氧化氢酶[mL/(g∙24h)] | 转化酶[mg/(g∙24h)] |
| 1 | 8.96 | 4.87 | 2.36 | 10.45 |
| 2 | 2.21 | 4.98 | 0.98 | 5.45 |
| 3 | 5.65 | 5.88 | 1.25 | 8.89 |
| 4 | 1.99 | 2.89 | 0.69 | 2.58 |
| 5 | 0.96 | 6.69 | 0.25 | 0.96 |
| 6 | 4.23 | 6.05 | 1.14 | 5.58 |
| 7 | 1.24 | 2.45 | 0.45 | 3.56 |
| 8 | 1.58 | 6.03 | 0.89 | 3.69 |
| 9 | 0.45 | 3.21 | 0.14 | 0.45 |
养殖池表层沉积物中重金属Cu、Zn、Pb、Cd、Cr、As、Mn的不同赋存形态和4种生物酶活性的相关关系见表 2。
| 元素 | 酶 | 形态分布 | |||||
| 可交换态 | 碳酸盐结合态 | 铁锰氧化物态 | 有机硫化物态 | 残渣态 | 总量 | ||
| Cu | 脲酶 | –0.560 | –0.127 | –0.823** | –0.507 | –0.603 | –0.662 |
| 碱性磷酸酶 | 0.168 | –0.151 | 0.179 | –0.097 | 0.334 | 0.205 | |
| 过氧化氢酶 | –0.486 | –0.276 | –0.828** | –0.520 | –0.530 | –0.639 | |
| 转化酶 | –0.708* | –0.123 | –0.735* | –0.454 | –0.604 | –0.627 | |
| Zn | 脲酶 | 0.130 | –0.135 | –0.501 | –0.715* | –0.554 | –0.684* |
| 碱性磷酸酶 | 0.603 | –0.582 | –0.660* | –0.591 | –0.579 | –0.540 | |
| 过氧化氢酶 | 0.173 | –0.324 | –0.520 | –0.734* | –0.545 | –0.701* | |
| 转化酶 | 0.039 | –0.205 | –0.330 | –0.675* | –0.389 | –0.572 | |
| Pb | 脲酶 | –0.172 | –0.609 | –0.169 | 0.942** | 0.197 | –0.343 |
| 碱性磷酸酶 | –0.388 | –0.268 | –0.274 | –0.245 | –0.909** | 0.400* | |
| 过氧化氢酶 | –0.121 | –0.462 | –0.136 | 0.894** | 0.100 | –0.236 | |
| 转化酶 | –0.052 | –0.571 | –0.122 | 0.919** | 0.040 | –0.199 | |
| Cd | 脲酶 | –0.675* | –0.685* | –0.699 | –0.814** | -0.656 | –0.731* |
| 碱性磷酸酶 | 0.109 | 0.984** | 0.823** | 0.730 | 0.850** | 0.977** | |
| 过氧化氢酶 | –0.753* | –0.750* | –0.779* | –0.835** | –0.753* | –0.805** | |
| 转化酶 | –0.797* | –0.805** | –0.810** | –0.828** | –0.806** | –0.851** | |
| Cr | 脲酶 | 0.258 | –0.013 | 0.182 | –0.119 | –0.001 | –0.012 |
| 碱性磷酸酶 | 0.812** | 0.648 | –0.146 | 0.087 | –0.742** | –0.715** | |
| 过氧化氢酶 | 0.187 | –0.120 | 0.258 | –0.157 | 0.036 | 0.034 | |
| 转化酶 | 0.261 | –0.037 | 0.240 | –0.008 | 0.061 | 0.080 | |
| As | 脲酶 | -0.717* | –0.509 | –0.831** | –0.418 | –0.650 | –0.803** |
| 碱性磷酸酶 | –0.241 | 0.635 | 0.539 | 0.502 | 0.407 | 0.566 | |
| 过氧化氢酶 | –0.635 | –0.438 | –0.829** | –0.534 | –0.642 | –0.775* | |
| 转化酶 | –0.736* | –0.471 | –0.768* | –0.510 | –0.757* | –0.858** | |
| Mn | 脲酶 | 0.495 | 0.345 | 0.363 | 0.809** | 0.405 | 0.398 |
| 碱性磷酸酶 | –0.088 | –0.145 | –0.118 | –0.002 | –0.109 | –0.118 | |
| 过氧化氢酶 | 0.366 | 0.193 | 0.203 | 0.774* | 0.251 | 0.245 | |
| 转化酶 | 0.385 | 0.230 | 0.262 | 0.667* | 0.298 | 0.290 | |
| *表示双侧检验P<0.05; **表示双侧检验P<0.01 | |||||||
重金属Cu和Zn以有机-硫化物结合态为主要的赋存形态,所占的含量比例为47.58%和34.23%。重金属元素的有机结合态是指土壤中和各种有机物螯合的那部分金属,水生生物活动及人类排放富含有机物的污水对其含量贡献较大,有研究表明在氧化环境和pH值升高的情况下可能被释放,引起生物毒性效应(隆茜等,2002)。Cu的可交换态、碳酸盐结合态、铁锰氧化物态、残渣态占的百分比例分别为: 8%、8.78%、14.66%、20.97%,Zn的可交换态、碳酸盐结合态、铁锰氧化物态、残渣态占的百分比例分别为:9.65%、11.08%、25.98%、19.05%。重金属Pb以铁锰氧化物态为主要的赋存形态(平均百分比为47.95%)。重金属的铁锰氧化物态是指吸附在活性的铁锰氧化物表面的那部分金属,反映人类活动对环境的污染。环境pH值较高时有利于铁锰氧化物的形成,在还原条件下易溶解释放而被生物利用。Pb的其它赋存形态百分比分别为: 5.42%(可交换态)、21.36%(碳酸盐结合态)、12.53%(有机-硫化物态)、12.70%(残渣态)。重金属Cd以可交换态(平均33.47%)和碳酸盐结合态(平均31.16%)为主要存在形态,其它形态所占百分比较低(铁锰氧化物态为13.46%、有机-硫化物态为8.68%、残渣态为13.24%)。可交换态指吸附在粘土、腐殖质上的金属,对环境变化敏感,易于迁移转化,反映人类近期排污活动对生物毒性作用。碳酸盐结合态指重金属元素在碳酸盐矿物上形成的共沉淀结合态,对环境中的pH值最为敏感,pH值低时易于重新释放到环境。重金属Cr和As主要以残渣态存在,所占比例分别为88.94%和70.13%,可交换态和碳酸盐结合态、有机结合态所占比例都较低,分别为1.88%、1.78%、2.22%和4.22%、4.19%、3.67%。金属残渣态一般长期稳定在沉积物中,不易释放,不被生物利用吸收。重金属Mn的铁锰氧化物态比例最高,为平均46.27%,其次为碳酸盐结合态(平均27.04%),余下依次为残渣态(平均19.06%)、可交换态(平均4.97%)、有机-硫化物态(平均2.68%)。
3.2 养殖池表层沉积物中酶活性水平脲酶、碱性磷酸酶和转化酶同属水解酶,水解酶活性高低取决于内源污染和外源污染的共同作用,可以指示富营养化程度(张宇等,2011)。有研究表明,沉积物中脲酶活性和氨氮含量呈显著正相关,可反映沉积物中无机氮的供应能力(张宇等,2011)。碱性磷酸酶能够催化沉积物中有机磷向无机磷的转化反应,与有机质和总氮呈正相关(刘存歧等,2007)。转化酶活性不仅取决于土壤有机质的含量,更多取决于土壤的有机质类型(周礼恺,1987),可作为表征土壤肥力的重要指标(张银龙等,1999)。过氧化氢酶是沉积物中常见的氧化还原酶,在有机质降解和腐殖质形成过程中具有重要作用,可以表示沉积物氧化过程的强度(Hakulinen et al,2005)。本研究发现,连云港海水养殖池表层沉积物中脲酶活性与重金属Zn、Cd、As总浓度呈显著负相关关系(见表 2);碱性磷酸酶活性与重金属Pb、Cd总浓度显著正相关,而与Cr总浓度显著负相关;过氧化氢酶活性与重金属Zn、Cd、As总浓度呈显著负相关关系;转化酶活性与重金属Cd、As总浓度显著负相关。生物酶活性和重金属总浓度呈现负相关表示高浓度的重金属污染抑制了生物酶的活性,进而导致沉积环境中营养物质的转化受到抑制,沉积物质量受到负面效应的影响。我们的研究结果初步表明,脲酶、过氧化氢酶、转化酶的活性明显受到重金属Cd的抑制,反过来讲,这三种酶活性可以表征重金属Cd的污染变化,进而可以评价沉积环境质量状况。
3.3 养殖池表层沉积物中重金属赋存形态和生物酶活性相关性分析由表 2可见,对于重金属Cu,其可交换态与转化酶活性呈显著负相关,而铁锰氧化物态与脲酶、过氧化氢酶、转化酶活性同样呈显著负相关,即当沉积物中转化酶活性高时,可交换态Cu向其他形态进行转化,降低了生物利用度,而当脲酶、过氧化氢酶、转化酶的活性较高时,出现了铁锰氧化物结合态的Cu向其他形态转化的现象;对于Zn,铁锰氧化物态与碱性磷酸酶活性显著负相关,有机结合态与脲酶、过氧化氢酶、转化酶活性显著负相关,说明当沉积物中碱性磷酸酶活性高时,铁锰氧化物态Zn含量降低,而当脲酶、过氧化氢酶、转化酶活性较高时,有机结合态含量Zn降低,开始向其他形态转化。有机结合态的Pb和脲酶、过氧化氢酶、转化酶活性呈显著正相关,表明当此三种酶活性增强时,沉积物中的Pb向有机结合态转化。而当碱性磷酸酶活性增强时,沉积物中的Pb则向残渣态转变,降低了生物利用度。重金属Cd的5种赋存形态和生物酶活性关系非常显著,这可能和Cd主要以可交换态存在,向环境中的释放量大,生物利用度高有关。Cr的可交换态和碱性磷酸酶活性显著正相关,残渣态和碱性磷酸酶活性显著负相关,即说明碱性磷酸酶活性高时,主要的存在形态残渣态含量减低,并开始向可交换态转化。重金属As的不同赋存形态与生物酶活性有显著相关关系的都表现为负相关,说明酶活性的改变可以表征养殖池沉积物中As的形态转化,进而影响As的生物有效性。重金属Mn的有机结合态和脲酶、过氧化氢酶、转化酶活性呈显著正相关,即脲酶、过氧化氢酶、转化酶活性增强时,沉积物中Mn的有机结合态含量上升。
综上所述,由于海水养殖池环境是相对封闭的,其沉积物中生物酶活性在土壤性质、生物活动及外源污染的共同影响下,与重金属总量及赋存形态呈现明显的多重相关关系,一方面说明了重金属浓度变化会刺激或者抑制生物酶活性,另一方面也可以利用生物酶的活性变化来指示沉积环境中重金属赋存形态间的相互转化。但通过本次调查,并未发现生物酶活性和重金属赋存形态间的特异性关系,值得进一步研究探讨。
4 结论2014年9月的调查结果表明,连云港市对虾养殖区养殖池表层沉积物中重金属Cu和Zn以有机-硫化物结合态为主要的赋存形态,Pb以铁锰氧化物态为主要的赋存形态,Cd以可交换态和碳酸盐结合态为主要存在形态,Cr和As主要以残渣态存在,Mn的铁锰氧化物态比例最高。重金属Cd最易于迁移转化,生物利用程度高。养殖区表层沉积物中生物酶活性空间差异性大,通过和重金属含量相关性分析发现脲酶、过氧化氢酶、转化酶的活性明显受到重金属Cd的抑制作用。
表层沉积物中重金属不同赋存形态与酶活性存在一定的相关性,但未表现出明显的特异性关系。脲酶活性与Cd、As的可交换态、Cd的碳酸盐结合态、Cu、As的铁锰氧化物态、Zn、Pb、Cd、Mn的有机硫化物态之间显著相关;碱性磷酸酶活性与Zn、Cd的铁锰氧化物态呈显著相关关系;过氧化氢酶活性与Cd的可交换态、碳酸盐结合态及残渣态、Cu、Cd、As的铁锰氧化物态、Zn、Pb、Cd、Mn的有机硫结合态之间显著相关;转化酶活性与Cu、Cd、As的可交换态、Cd的碳酸盐结合态、Cu、Cd、As的铁锰氧化物态、Zn、Pb、Cd、Mn的有机硫化物态、Cd、As的残渣态之间显著相关。研究结果表明,酶活性变化可以用来指示沉积物中重金属的形态转化过程。
| 王小静,李力,高晶晶等, 2015.渤海西南部近岸功能区表层沉积物重金属形态分析及环境评价.海洋与湖沼, 46(3):517-525 |
| 史长青, 1995.重金属污染对水稻土酶活性的影响.土壤通报, 26(1):34-35 |
| 刘霞,刘树庆,王胜爱, 2002.河北主要土壤中重金属镉、铅形态与土壤酶活性的关系.河北农业大学学报, 25(1):33-37, 60 |
| 刘霞,刘树庆,唐兆宏, 2003.潮土和潮褐土中重金属形态与土壤酶活性的关系.土壤学报, 40(4):581-587 |
| 刘云国,李欣,徐敏等, 2002.土壤重金属镉污染的植物修复与土壤酶活性.湖南大学学报(自然科学版), 29(4):108-113 |
| 刘存歧,陆健健,李贺鹏, 2007.长江口潮滩湿地土壤酶活性的陆向变化以及与环境因子的相关性.生态学报, 27(9):3663-3669 |
| 关松荫, 1986.土壤酶及其研究法.北京:农业出版社, 274-300 |
| 李越蜀,郑忠明,翟海佳等, 2012.不同模式凡纳滨对虾(Litopenaeus vannamei)养殖池塘沉积物酶活性及其微生物群落结构分析.海洋与湖沼, 43(6):1254-1260 |
| 宋科,赵晟,张力等, 2013.于模糊综合评价法的东极大黄鱼(Larimichthys crocea)养殖区海水水质评价.海洋与湖沼, 44(2):383-388 |
| 张宇,乌恩,李重祥等, 2011.长江中下游湖泊沉积物酶活性及其与富营养化的关系.应用与环境生物学报, 17(2):196-201 |
| 张银龙,林鹏, 1999.秋茄红树林土壤酶活性时空动态.厦门大学学报(自然科学版), 38(1):129-136 |
| 周礼恺, 1987.土壤酶学.北京:科学出版社, 106-221 |
| 赵兰坡,姜岩, 1986.土壤磷酸酶活性测定方法的探讨.土壤通报, 17(3):138-141 |
| 隆茜,张经, 2002.陆架区沉积物中重金属研究的基本方法及其应用.海洋湖沼通报, (3):25-35 |
| 蔡信德,仇荣亮,汤叶涛等, 2005.外源镍在土壤中的存在形态及其与土壤酶活性的关系.中山大学学报(自然科学版), 44(5):93-97 |
| 廖红芳,郑忠明,冯坚等, 2014.象山港大黄鱼(Pseudosciaena crocea)网箱养殖区及邻近海域沉积物中异养细菌生态分布.海洋与湖沼, 45(6):1308-1316 |
| Choi K Y, Kim S H, Hong G H et al, 2012. Distributions of heavy metals in the sediments of South Korean harbors. Environmental Geochemistry and Health, 34(S1):71-82 |
| Colin V L, Villegas L B, Abate C M, 2012. Indigenous microorganisms as potential bioremediators for environments contaminated with heavy metals. International Biodeterioration & Biodegradation, 69:28-37 |
| De Souza M J, Nair S, Loka Bharathi P A et al, 2006. Metal and antibiotic-resistance in psychrotrophic bacteria from Antarctic marine waters. Ecotoxicology, 15(4):379-384 |
| Dick R P, 1997. Soil enzyme activities as integrative indicators of soil health. In:Pankhurst C E, Doube B M, Gupta V V S R eds. Biological Indicators of Soil Health. New York, USA:CAB International, 121-156 |
| Elzobair K A, Stromberger M E, Ippolito J A, 2016. Stabilizing effect of biochar on soil extracellular enzymes after a denaturing stress. Chemosphere, 142:114-119 |
| Ghosh A K, Bhattacharyya P, Pal R, 2004. Effect of arsenic contamination on microbial biomass and its activities in arsenic contaminated soils of Gangetic West Bengal, India. Environmental International, 30(4):491-499 |
| Gianfreda L, Rao M A, Piotrowska A et al, 2005. Soil enzyme activities as affected by anthropogenic alterations:intensive agricultural practices and organic pollution. Science of the Total Environment, 341(1-3):265-279 |
| Haferburg G, Kothe E, 2010. Metallomics:lessons for metalliferous soil remediation. Applied Microbiology and Biotechnology, 87(4):1271-1280 |
| Hakulinen R, Kähkönen M A, Salkinoja-Salonen M, 2005. Vertical distribution of sediment enzyme activities involved in the cycling of carbon, nitrogen, phosphorus and sulphur in three boreal rural lakes. Water Research, 39(11):2319-2326 |
| Hendriksen N B, Creamer R E, Stone D et al, 2016. Soil exo-enzyme activities across Europe-the influence of climate, land-use and soil properties. Applied Soil Ecology, 97:44-48 |
| Hiroki M, 1993. Effect of arsenic pollution on soil microbial population. Soil Science and Plant Nutrition, 39(2):227-235 |
| Ho H H, Swennen R, Cappuyns V et al, 2013. Assessment on pollution by heavy metals and arsenic based on surficial and core sediments in the Cam river mouth, Haiphong Province, Vietnam. Soil and Sediment Contamination, 22(4):415-432 |
| Hu R, Wang X P, Zhang Y F et al, 2016. Insight into the influence of sand-stabilizing shrubs on soil enzyme activity in a temperate desert. CATENA, 137:526-535 |
| Kavamura V N, Esposito E, 2010. Biotechnological strategies applied to the decontamination of soils polluted with heavy metals. Biotechnology Advances, 28(1):61-69 |
| Li Z J, Xu J M, Tang C X et al, 2006. Application of 16S rDNA-PCR amplification and DGGE fingerprinting for detection of shift in microbial community diversity in Cu-, Zn-, and Cd-contaminated paddy soils. Chemosphere, 62(8):1374-1380 |
| Lorenz N, Hintemann T, Kramarewa T et al, 2006. Response of microbial activity and microbial community composition in soils to long-term arsenic and cadmium exposure. Soil Biology and Biochemistry, 38(6):1430-1437 |
| Rauret G, 1998. Extraction procedures for the determination of heavy metals in contaminated soil and sediment. Talanta, 46(3):449-455 |
| Rutgers M, Wouterse M, Drost S M et al, 2016. Monitoring soil bacteria with community-level physiological profiles using BiologTM ECO-plates in the Netherlands and Europe. Applied Soil Ecology, 97:23-35 |
| Sivakumar S, Nityanandi D, Barathi S et al, 2012. Selected enzyme activities of urban heavy metal-polluted soils in the presence and absence of an oligochaete, Lampito mauritii (Kinberg). Journal of Hazardous Materials, 227-228:179-184 |
| Sobolev D, Begonia M F, 2008. Effects of heavy metal contamination upon soil microbes:lead induced changes in general and denitrifying microbial communities as evidenced by molecular markers. International Journal of Environmental Research and Public Health, 5(5):450-456 |
| Talbot J M, Bruns T D, Taylor J W et al, 2014. Endemism and functional convergence across the North American soil mycobiome. Proceedings of the National Academy of Sciences of the United States of America, 111(17):6341-6346 |
| Tessier A, Campbell P G C, Bisson M, 1979. Sequential extraction procedure for the speciation of particulate trace metals. Analytical Chemistry, 51(7):844-851 |
| Valsecchi G, Gigliotti C, Farini A, 1995. Microbial biomass, activity, and organic matter accumulation in soils contaminated with heavy metals. Biology and Fertility of Soils, 20(4):253-259 |
| Walker C, Goodyear C, Anderson D et al, 2000. Identification of Arsenic resistant bacteria in the soil of a former munitions factory at Löcknitz, Germany. Land Contamination & Reclamation, 8(1):13-18 |
| Wang X S, Wang S J, Zhu G C et al, 2011. A statistical approach for assessing heavy metal contamination in near-shore marine sediment cores:a case study from the Yellow Sea, China. International Journal of Environmental Studies, 68(1):73-82 |
| Wang Y P, Shi J Y, Wang H et al, 2007. The influence of soil heavy metals pollution on soil microbial biomass, enzyme activity, and community composition near a copper smelter. Ecotoxicology and Environmental Safety, 67(1):75-81 |
| Yu K C, Tsai L J, Chen S H et al, 2001. Chemical binding of heavy metals in anoxic river sediments. Water Research, 35(17):4086-4094 |
| Zhang R, Zhang F, Ding Y J et al, 2013. Historical trends in the anthropogenic heavy metal levels in the tidal flat sediments of Lianyungang, China. Journal of Environmental Sciences, 25(7):1458-1468 |
| Zhang W F, Liu X P, Cheng H F et al, 2012. Heavy metal pollution in sediments of a typical mariculture zone in South China. Marine Pollution Bulletin, 64(4):712-720 |
| Zhu H N, Yuan X Z, Zeng G M et al, 2012. Ecological risk assessment of heavy metals in sediments of Xiawan Port based on modified potential ecological risk index. Transactions of Nonferrous Metals Society of China, 22(6):1470-1477 |
 2016, Vol. 47
2016, Vol. 47

