中国海洋湖沼学会主办。
文章信息
- 谢利, 王朝阳, 张迪骏, 周君, 司开学, 张红燕, 韩姣姣, 崔晨茜, 董丽莎, 苏秀榕. 2016.
- XIE Li, WANG Zhao-Yang, ZHANG Di-Jun, ZHOU Jun, SI Kai-Xue, ZHANG Hong-Yan, HAN Jiao-Jiao, CUI Chen-Qian, DONG Li-Sha, SU Xiu-Rong. 2016.
- 宁波沿海陆源排污口蓝藻(Cyanobacteria)和裸藻纲(Euglenoidea)生物的分布特点
- CYANOBACTERIA AND EUGLENOIDEA DISTRIBUTION IN SEWAGE OUTLETS ALONG NINGBO COAST
- 海洋与湖沼, 47(1): 188-194
- Oceanologia et Limnologia Sinica, 47(1): 188-194.
- http://dx.doi.org/10.11693/hyhz20140600180
-
文章历史
- 收稿日期: 2014-06-25
- 收修改稿日期: 2015-01-28
2. 宁波大学海洋学院 宁波 315211
2. School of Marine Sciences, Ningbo University, Ningbo 315211, China
蓝藻(Cyanobacteria)又称为蓝细菌或蓝绿藻,是一类进化历史悠久、革兰氏染色阴性、无鞭毛、含叶绿素a(但不形成叶绿体)、能进行产氧性光合作用的大型原核微生物。蓝藻的分布广泛,从水生到陆生生态系统,从热带到南北极均有分布。蓝藻是海洋生态系统和海洋初级生产力的重要组成部分(孙晟等,2003; Paul,2008)。蓝藻结构简单,细胞内没有真正的细胞核结构和色素体,只有核质和色素两大部分。蓝藻的繁殖方式有两类,一类为营养繁殖,包括细胞直接分裂(即裂殖)、群体破裂和丝状体产生藻殖段等几种方法; 另一类为可产生内生孢子或外生孢子等,以进行无性生殖。蓝藻主要有微囊藻、螺旋藻、项圈藻、颤藻等,其中微囊藻的危害最大(Asselman et al,2014)。根据长期的观测,发现在大多数情况下,在特定湖区内,这种突然“暴发”的水华是在适宜的气象与水文条件下,该湖区内亦已存在的、悬浮于水体中的蓝藻群体再加上其它湖区的水华蓝藻,随着风和湖流的驱动,漂移到该湖区聚集上浮至水面,并为人们肉眼所见的过程(孔繁翔等,2009; O’Neil et al,2012)。蓝藻作为河湖水华中的常见优势种群,引起的蓝藻事件是目前社会普遍关注的问题。蓝藻水华的暴发是水体富营养化特征之一。蓝藻通过产生毒素、死亡个体分解使水体缺氧和破坏正常的食物链威胁到饮用水安全、公众健康和景观,会造成严重的经济损失和社会问题(马健荣等,2013)。因此人们开始关注蓝藻,并取得一定的进展。眼虫门是一群鞭毛生物,兼有叶绿素和眼点,兼有动物和植物的特性,在植物学、藻类学中称为“裸藻”,而在原生动物学中称为“眼虫”,因此眼虫门也称作裸藻门。眼虫门主要有两个纲: 裸藻纲和动质体纲。在本次研究中的主要对象是裸藻纲,这类生物在水华和赤潮中也起一定的作用。
藻-菌关系一直是研究的热点问题之一,但目前主要集中在海洋、湖泊赤潮藻方面,陆源排污口中的蓝藻和裸藻纲生物未见报道。本文选取宁波沿海10个主要的陆源排污口,分别对排污口处和距排污口50m以外的20个站位的水样进行分析,对每个站点进行总体和单独分析,研究蓝藻和裸藻纲生物种类和分布特点。
1 材料与方法 1.1 样品采集选取宁波沿海10个陆源排污口和距离排污口50m以外的10个站位作为采样位点(见图 1)。分别于2011年3月、5月、8月、10月进行采集,每次采集4L水样。
 |
| 图 1 采样站位区域分布图 Fig. 1 Map of sampling site S1: 象山爵溪东塘排污口; S2: 象山水桶岱垃圾场排污口,S3: 象山石浦水产加工园区排污口,S4: 象山西周工业园区排污口,S5: 象山墙头综合排污口,S6: 北仑三山排污口,S7: 宁海西店崔家综合排污口,S8: 奉化下陈排污口,S9: 宁海颜公河入海排污口,S10: 余姚黄家埠排污口; 其中S5和S9为重点排污口,其余为一般排污口 |
取排污口的海水,以0.22μm的微孔滤膜富集微生物,利用试剂盒提取基因组 DNA(美国Omega生物技术公司)。
1.2.2 PCR扩增根据细菌16S rRNA的保守序列,利用Primer Premier 5.0设计扩增引物: 16S F(5’-CCA TCT CAT CCC TGC GTG TCT CCG ACT CAG-3’)和16S R(5’-CCT ATC CCC TGT GTG CCT TGG CAG TCT CAG-3’)。
20μL扩增反应体系: 10×buffer 2μL,MgCl2 2μL,dNTP 2μL,上游引物和下游引物各25μL,0.2μL Taq DNA聚合酶和1μL DNA模版。PCR扩增产物用2%的琼脂糖凝胶电泳检测(Wang et al,2014a,b)。
PCR扩增条件: 94℃预变性4 min,94℃变性30 s,退火温度从65℃到55℃,退火30 s,20个循环; 72℃延伸30 s,94℃变性30 s,55℃退火30 s,72℃延伸30s,35个循环; 最终72℃延伸10 min(刘兵等,2009)。
1.2.3 测序与分析将纯化后的PCR产物进行454焦磷酸测序(Margulies et al,2005; 王中华等,2014),结果用罗氏软件2.5.3进行信号处理分析。根据蓝藻细菌在文库中出现的频次数量,进一步用R For Window 2.15.2、SPSS等进行统计分析。
2 结果与分析 2.1 454测序分析裸藻纲和蓝藻在排污口的分布通过对454高通量测序共检出眼虫门的裸藻纲(Euglenoidea)、蓝藻门的集球藻目(Synechococcophycideae)、颤藻目(Oscillatoriophycideae)、念珠藻目(Nostocophycideae)、粘杆菌目(Gloeobacterophycideae),具体数量见表 1。
| 检出菌种 | 检出频次(%,总和) | 检出频次(%,3月) | 检出频次(%,5月) | 检出频次(%,8月) | 检出频次(%,10月) |
| 裸藻纲 | 29305(82.745) | 17504(88.312) | 3485(85.027) | 5928(75.240) | 2387(65.997) |
| 集球藻目 | 2020(5.704) | 22(0.111) | 74(1.805) | 1114(14.139) | 810(22.394) |
| 颤藻目 | 633(1.787) | 325(1.640) | 44(1.073) | 143(1.815) | 121(3.345) |
| 念珠藻目 | 224(0.632) | 42(0.212) | 112(2.732) | 35(0.444) | 35(0.968) |
| 粘杆菌目 | 7(0.020) | 0(0) | 0(0) | 6(0.076) | 1(0.028) |
通过对454高通量测序平台结果进行比对分析发现: 在3月份,S4象山西周工业园区排污口、S7宁海西店崔家综合排污口蓝藻和裸藻纲生物数量最多,S7宁海西店崔家综合排污口次之。在5月份,S4象山西周工业园区排污口的检出次数最高,S6北仑三山排污口、S7宁海西店崔家综合排污口和S8奉化下陈排污口次之。在8月份,S7宁海西店崔家综合排污口的检出次数最高,S9宁海颜公河入海排污口次之。在10月份,S6北仑三山排污口检出次数最高,S7宁海西店崔家综合排污口和S9宁海颜公河入海排污口次之。
3月份的蓝藻和裸藻纲生物检出次数最高,8月份和10月份检出次数较低。其原因是8月份东海海洋表面平均温度达到年最高值约为30—35℃,高温使部分工厂停产休息,因此污水排放量减小(陈丽萍等,2013),3月份的时候排污量较多,而且气温较低适于这两类生物的生长,因此检出次数与季节温度、空气湿度有关(图 2)。
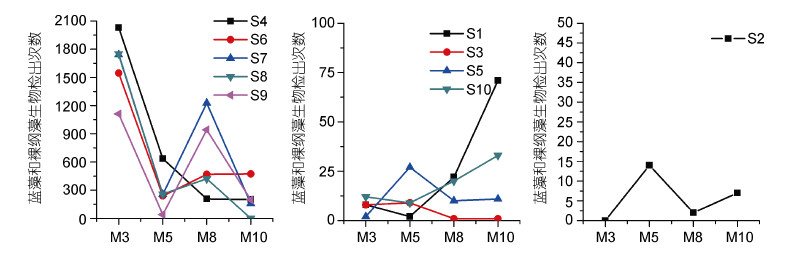 |
| 图 2 不同月份蓝藻和裸藻纲生物在排污口的分布情况 Fig. 2 The distribution of Cyanobacteria and Euglenoidea in different sewage outlets and months |
3月份,距S7宁海西店崔家综合排污口50m处蓝藻和裸藻纲生物数量最多,距S4象山西周工业园区排污口50m处含量次之; 5月份,距S7宁海西店崔家综合排污口50m处含量最高,距S4象山西周工业园区排污口50m处含量次之; 8月份,距S7宁海西店崔家综合排污口50m处含量最高,距S6北仑三山排污口50m处含量次之; 10月份,距S6北仑三山排污口50m处含量最高,距S7宁海西店崔家综合排污口50m处含量次之(图 3)。
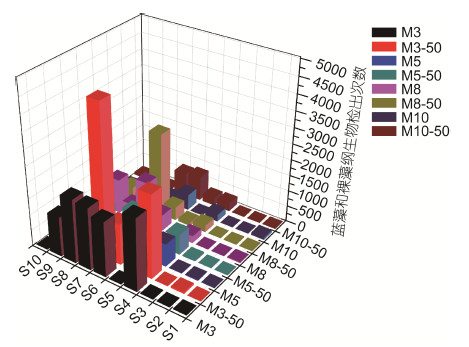 |
| 图 3 不同月份各排污口的蓝藻和裸藻纲生物数量与50m的站位点的比较 Fig. 3 Comparison in Cyanobacteria and Euglenoidea quantity between each sewage outlet and a site 50m away in different months M3,M5,M8,M10分别表示3,5,8,10月份排污口站位; M3-50,M5-50,M8-50,M10-50分别表示3,5,8,10月份距排污口50m以外的站位 |
蓝藻和裸藻纲生物大量出现时,附近水体一般呈蓝色或绿色,水面被大量藻体覆盖。蓝藻细胞尤其是微囊藻将毒素释放到水里,由于本身的机制使得其在夏天的富营养水体中容易大量暴发生长,造成严重的水体生态灾难(Bresciani et al,2014)。微囊藻毒素对人体肝功能有很大的伤害,生活在湖边、池塘边和海边的人容易通过饮用水和食用藻类中毒(王伟琴等,2010; Urrutia-Cordero et al,2013)。宁海西店镇是中国著名的“牡蛎之乡”,牡蛎营养丰富,具有各种人体必需氨基酸对降低血糖也有一定的作用(滕瑜等,2005),冬季是西店牡蛎最盛产也是蛎肉最肥美的季节。而蛎肉品质与海水的质量有着紧密联系,某些蓝细菌(如集球藻目)会通过内吞的方式进入牡蛎组织内部达到寄生目的,进而在牡蛎组织内部累积,从而污染了牡蛎的肉质(Avila-Poveda et al,2014),因此3月份应重点加强对S7号排污口的监控,以免造成牡蛎污染和经济损失。
2.3 种类的分布在3月份,S4号象山西周工业园区排污口裸藻纲生物检出频次最高(排污口1906次,距排污口50m处2223次),占3月份所有检出生物总量的20.83%,蓝藻检出频次则较少(排污口124次,距排污口50m处106次); S2号象山水桶岱垃圾场排污口中两类生物排出量最少(排污口0次,距排污口50m处51次)。说明S2号3月份排污口排出的污染物中没有这两类微生物需要的营养。而其它排污口均是裸藻纲生物的检出频次最高(图 4)。在5月份,各排污口蓝藻检出频次均较少,S4号象山西周工业园区排污口裸藻纲生物检出频次最高(排污口629次,距排污口50m处557次),S6号北仑三山排污口裸藻纲生物检出频次也较高(排污口处231次,距排污口50m处343次),S1号象山爵溪东塘排污口裸藻纲生物检出频次最低(排污口处3次,距排污口50m处3次)。在8月份,S7号宁海西店崔家综合排污口裸藻纲生物检出频次最高(排污口处1077次,距排污口50m处2040次),其它排污口裸藻纲生物检出频次都较低。各排污口集球藻目检出频次均偏低,其中S8号奉化下陈排污口检出频次最高(排污口处236次,距排污口50m处4次),S6号北仑三山排污口集球藻目检出频次次之(排污口处180次,距排污口50m处195次)。而S2、S3、S5号则没有集球藻目。在10月份,S6号北仑三山排污口集球藻目检出次数最高(排污口处344次,距排污口50m处249次),而裸藻纲检出频次较低(排污口处129次,距排污口50m处404次),S9宁海颜公河入海排污口叶绿体目检出频次最高(排污口212次,距排污口50m处193次),集球藻目检出次数则较低。
 |
| 图 4 不同月份和不同站位排污口的蓝藻和裸藻纲生物检出次数 Fig. 4 The numbers of Cyanobacteria and Euglenoidea in the sewage outlets in different months M3,M5,M8,M10分别表示3,5,8,10月份排污口站位; M3-50,M5-50,M8-50,M10-50分别表示3,5,8,10月份距排污口50m以外的站位 |
S7宁海西店崔家综合排污口和距排污口50m处裸藻纲生物的检出次数总数最高,说明S7号处的海水质量更适合裸藻纲生物的生长。宁海西店崔家综合排污口的主要污染物没有氨氮化合物,而其它排污口处氨氮浓度较高。裸藻纲生物的生长并不只是受氨氮含量的影响,氮磷比对裸藻纲生物的生长影响较大,在低磷情况下(0.02mg/L),氮磷比为4︰1—32︰1范围内,某些生物(如铜绿微囊藻和斜生栅藻)的生长均受到营养盐的限制,当磷浓度达到0.20mg/L时,这两种藻类分别在在N/P比为32︰1和64︰1时生长速率达到最大值,而在磷浓度升高到2mg/L时,氮磷比对生长速率已经没有影响(Sabour et al,2009; 许海等,2011)。可以推测S7号排出的污水中氮磷比适合裸藻纲生物的生长,因此应该加强对S7号氮磷含量的监控,以避免出现水华现象(图 4)。
2.4 蓝藻和裸藻纲生物在重点排污口的分布S9号宁海颜公河入海排污口和S5号象山墙头综合排污口为宁波市两个重点沿海排污口。两类生物检出频次在时间和数量上有明显的差异。S9号宁海颜公河入海排污口中的裸藻纲检出频次最高为3月份,高达1099次,最低为5月份的35次,蓝藻的检出次数在3、5、8、10月份检出频次均很少,最高为8月份16次。S5号象山墙头综合排污口裸藻纲检出频次最高为5月份,高达23次,其它月份排污口裸藻纲的检出频次都在15次以下,而蓝藻在四个月份检出频次一共只有3次(图 5)。S9号宁海颜公河入海排污口和S5号象山墙头综合排污口排出的主要是裸藻纲。
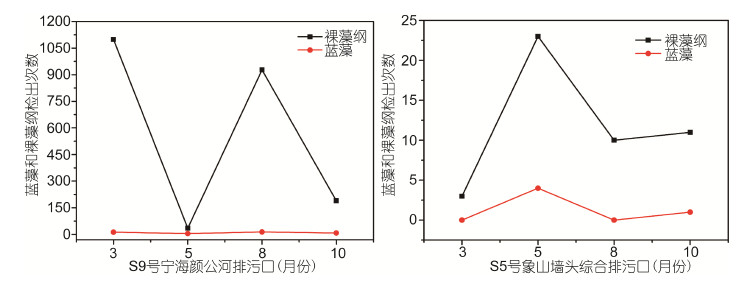 |
| 图 5 重点排污口蓝藻和裸藻纲生物各月份检出频次 Fig. 5 The number of Cyanobacteria and Euglenoidea in major sewage outlets in different months |
S9号宁海颜公河入海排污口的主要污染物为磷和氨氮,S5号象山墙头综合排污口的主要污染为粪大肠菌群、苯胺、生化需氧量。这两个重点排污口两类生物检出频次均相对较少,说明这两个排污口污染物中氮磷比含量不适合它们生长。但是宁海颜公河排污口和象山墙头综合排污口分别在3月和5月裸藻纲的检出量达到最大值,宁海颜公河排污口3月份裸藻纲检出频次要高于象山墙头综合排污口在5月份的检出频次,这可能与宁波3月份和5月份气温有关系,3月份平均气温比5月份平均气温低10℃左右,推测裸藻纲生物更适宜较低温度生长; 蓝藻检出量分别在8月和5月达到最大值。宁波8月份日均最低温度为25℃,日均最高温度为32℃; 5月份日均最低温度为17℃,日均最高温度为25℃,铜绿微囊藻在15℃的生长速率和生长量低于在20℃、25℃下的生长速率,20℃条件下铜绿微囊藻在前期的生长速率低于在25℃下的生长速率,而在17d时两种条件下的生长量开始相等。铜绿微囊藻更容易在5月份生长,所以应根据温度变化做好对蓝藻生长的防治,以免其毒素在水产品中(如藻类、螺类、贝类和各种鱼类)积累,对人类健康造成危害(陈建中等,2010)。
3 结论利用454高通量测序技术,确定了宁波沿海2个重点排污口、8个一般排污口的20个站位的海水中,含有叶绿体的裸藻纲生物检出量最高,蓝藻门的集球藻目次之。由于季节性的影响,排污口的污染物和温度也会发生相应的变化,进而影响蓝藻的生长。裸藻纲生物的检出量也受各排污口中氮磷比含量影响较大,不同的生物在不同的氮磷比的条件下生长速率也会不同,S7号排污口中污染源更适合裸藻纲生物的生长。S9号和S5号排污口作为宁波市两个重点陆源排污口,两种生物检出量均相对较低,分别在3月份和5月份裸藻纲检出量最大,8月和5月蓝藻检出量达到最大值,季节性温度变化会影响这两类生物的生长,应该依照不同季节和不同类型的排污口针对性地对蓝藻进行治理,防止造成水体污染。
| 马健荣,邓建明,秦伯强等, 2013.湖泊蓝藻水华发生机理研究进展.生态学报, 33(10):3020-3030 |
| 王中华,徐茂琴,谢利等, 2014.宁波沿海陆源排污口拟杆菌(Bacteroidetes)分布的特点.海洋与湖沼, 45(5):1030-1036 |
| 王伟琴,金永堂,吴斌等, 2010.水源水中微囊藻毒素的遗传毒性与健康风险评价.中国环境科学, 30(4):468-476 |
| 孔繁翔,马荣华,高俊峰等, 2009.太湖蓝藻水华的预防、预测和预警的理论与实践.湖泊科学, 21(3):314-328 |
| 刘兵,李太武,苏秀榕等, 2009.宁波北仑港冬季浮游细菌多样性研究.台湾海峡, 28(2):217-222 |
| 许海,朱广伟,秦伯强等, 2011.氮磷比对水华蓝藻优势形成的影响.中国环境科学, 31(10):1676-1683 |
| 孙晟,肖天,岳海东, 2003.秋季与春季东、黄海蓝细菌(Synechococcus spp.)生态分布特点.海洋与湖沼, 34(2):161-168 |
| 陈丽萍,侯付景,张迪骏等, 2013.宁波沿海陆源排污口假单胞菌属(Pseudomonas)分布特点.海洋与湖沼, 44(4):926-930 |
| 陈建中,刘志礼,李晓明等, 2010.温度、pH和氮、磷含量对铜绿微囊藻(Microcystis aeruginosa)生长的影响.海洋与湖沼, 41(5):714-718 |
| 滕瑜,王彩理, 2005.牡蛎的营养和降糖作用研究.海洋水产研究, 26(6):39-44 |
| Asselman J, Hochmuth J D, de Schamphelaere K A C, 2014. A comparison of the sensitivities of Daphnia magna and Daphnia pulex to six different cyanobacteria. Harmful Algae, 39:1-7 |
| Avila-Poveda O H, Torres-Ariño A, Girón-Cruz D A et al, 2014. Evidence for accumulation of Synechococcus elongatus (Cyanobacteria:Cyanophyceae) in the tissues of the oyster Crassostrea gigas (Mollusca:Bivalvia). Tissue and Cell, 46(5):379-387 |
| Bresciani M, Adamo M, de Carolis G et al, 2014. Monitoring blooms and surface accumulation of cyanobacteria in the Curonian Lagoon by combining MERIS and ASAR data. Remote Sensing of Environment, 146:124-135 |
| Margulies M, Egholm M, Altman W E et al, 2005. Genome sequencing in microfabricated high-density picolitre reactors. Nature, 437(7057):376-380 |
| O'Neil J M, Davis T W, Burford M A et al, 2012. The rise of harmful cyanobacteria blooms:the potential roles of eutrophication and climate change. Harmful Algae, 14:313-334 |
| Paul V J, 2008. Global warming and cyanobacterial harmful algal blooms. Advances in Experimental Medicine and Biology, 619:239-257 |
| Sabour B, Loudiki M, Vasconcelos V, 2009. Growth responses of Microcystis ichthyoblabe Kützing and Anabaena aphanizomenoides Forti (cyanobacteria) under different nitrogen and phosphorus conditions. Chemistry and Ecology, 25(5):337-344 |
| Urrutia-Cordero P, Agha R, Cirés S et al, 2013. Effects of harmful cyanobacteria on the freshwater pathogenic free-living amoeba Acanthamoeba castellanii. Aquatic Toxicology, 130-131:9-17 |
| Wang Z H, Yang J Q, Zhang D J et al, 2014a. Composition of microbial communities in industrial drain outlets. Journal of Pure and Applied Microbiology, 8(1):807-815 |
| Wang Z H, Yang J Q, Zhang D J et al, 2014b. Composition and structure of microbial communities associated with different domestic sewage outfalls. Genetics and Molecular Research, 13(3):7542-7552 |
 2016, Vol. 47
2016, Vol. 47


